题目内容
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}(相对分子质量:288),可由乳酸与FeCO3反应制得,它易溶于水,几乎不溶于乙醇,是一种很好的补铁剂,但其水溶液易被氧化,光照可促进氧化。
I.制备碳酸亚铁:装置如图所示。
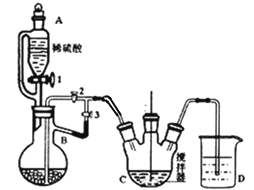
锌铁 NH4HCO3溶液
(1)仪器B的名称是________。
(2)实验操作如下:关闭活塞2,打开活塞1、3,加入适量稀硫酸反应一段时间,其目的是____________________________,然后关闭活塞1,接下来的操作是____________________,此后,C装置溶液中有沉淀生成,并有大量气泡冒出,则C中发生反应的离子方程式为_____________________________________。
Ⅱ.制备乳酸亚铁:
(3)向纯净的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。该反应的加热方式为____________。为防止乳酸亚铁变质,在上述体系中还应加入适量铁粉。反应结束后,将所得溶液隔绝空气低温浓缩、_________、过滤、洗涤、干燥,得乳酸亚铁晶体。该晶体存放时应注意_________________________。
III.乳酸亚铁晶体纯度的测量:
(4)某同学查阅文献后,用(NH4)4Ce(SO4)4滴定法测定样品中Fe2+的含量并计算样品纯度(反应中Ce4+还原为Ce3+),他称取6.00g样品,配制成250.00mL溶液,取出25.00mL,用浓度为0.10mol·L-1的(NH4)4Ce(SO4)4标准溶液滴定至终点,消耗标准液20.00mL。则产品中乳酸亚铁晶体的纯度为________(以质量分数表示)。
【答案】蒸馏烧瓶 排尽装置内的空气,防止Fe2+被氧化 打开活塞2,关闭活塞3 Fe2++2HCO3-=FeCO3↓+CO2↑+H2O 水浴75℃加热 冷却结晶 避光、密封保存 96%
【解析】
利用铁与稀硫酸反应生成的氢气,将生成的硫酸亚铁溶液压入碳酸氢铵溶液中,从而制得碳酸亚铁;控制一定条件,碳酸亚铁与乳酸反应生成乳酸亚铁溶液,经冷却结晶制得乳酸亚铁晶体;因为亚铁具有还原性,可用氧化还原滴定法测定其纯度。
I.(1)仪器B是蒸馏烧瓶。
(2)关闭活塞2,打开活塞1、3时,稀硫酸与铁反应生成硫酸亚铁溶液和氢气,氢气可排出装置内空气,防止亚铁被氧化。然后关闭活塞1,打开活塞2,关闭活塞3,此时生成的氢气使蒸馏烧瓶中压强变大,硫酸亚铁溶液沿导管上升,经活塞2进入三颈烧瓶,进而发生反应生成碳酸亚铁沉淀和气体,故C中离子方程式为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O。
Ⅱ.(3)FeCO3固体溶于足量的乳酸溶液需要75℃、搅拌条件,可采用75℃水浴加热,同时加入适量铁粉防止亚铁被氧化。乳酸亚铁晶体含结晶水,只能使用冷却结晶方法,故将生成的乳酸亚铁溶液在隔绝空气条件下,经低温浓缩、冷却结晶、过滤、洗涤、干燥,得乳酸亚铁晶体。据题意,乳酸亚铁易被空气中氧气氧化,且光照可促进氧化,故保存乳酸亚铁晶体应密封、避光。
III.(4)滴定过程中发生反应Fe2++Ce4+=Fe3++Ce3+,得关系式[CH3CH(OH)COO]2Fe·3H2O ~ (NH4)4Ce(SO4)4。
25.00mL样品溶液中n(Fe2+)=n(Ce4+)=0.10mol·L-1×20.00×10-3L=2.000×10-3mol
6.00g样品中,n(Fe2+)=2.000×10-3mol×![]() =2.000×10-2mol
=2.000×10-2mol
产品中乳酸亚铁晶体的纯度=![]() =96%
=96%

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案