题目内容
在容积恒定的密闭容器中,一定量的SO2与1.1molO2发生反应: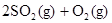
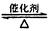
 。当气体的物质的量减少0.315mol时,反应达到平衡,SO2的平衡转化率是90%。下列说法正确的是
。当气体的物质的量减少0.315mol时,反应达到平衡,SO2的平衡转化率是90%。下列说法正确的是
| A.相同条件下,平衡时若充入稀有气体,SO2的转化率增大 |
| B.反应开始时,向容器中通入的SO2的物质的量是0.7mol |
| C.保持其他条件不变,仅降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| D.保持其他条件不变,仅缩小容器体积,反应达到平衡时容器中有1.485mol气体 |
B
解析试题分析:A、充入稀有气体,SO2、O2、SO3浓度不变,平衡不移动,SO2的转化率不变,错误;B、用差量法计算消耗的SO2的物质的量,再根据转化率计算反应开始时向容器中通入的SO2的物质的量,具体过程如下:
2SO2(g) + O2(g)=2SO3(g) △n
2 1
x 0.315mol
2/x="1/0.315mol" x=0.63mol
反应开始时,向容器中通入的SO2的物质的量n(SO2)=0.63mol/90%=0.7mol,正确;C、由于△H<0,所以降低温度平衡向右移动,证明正反应速率减小程度比逆反应速率减小程度小,所以正反应速率超过逆反应速率,错误 ;D、压缩前气体物质的量为0.7mol+1.1mol-0.315mol=1.485mol,但压缩后平衡向右移动,气体物质的量减少,小于1.485mol,错误。
考点:本题考查了化学平衡的计算。

图中表示外界条件(T、p)的变化对下列反应的影响:L(s)+G(g) 2R(g)△H>0,y 轴表示的是
2R(g)△H>0,y 轴表示的是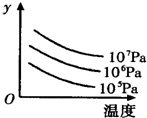
| A.平衡时,混合气中R的百分含量 | B.G的转化率 |
| C.平衡时,混合气中G的百分含量 | D.L的转化率 |
下列反应达到平衡后,升高温度可以使混合气体平均相对分子质量增大的是( )
A.H2(g)+I2(g)  2HI(g) ΔH<0 2HI(g) ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
C.N2(g)+3H2(g)  2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
D.2SO3(g) 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
在密闭容器中进行下列反应:M(g)+N(g) R(g)+2 L( ?),反应符合下图。下列叙述正确的是( )
R(g)+2 L( ?),反应符合下图。下列叙述正确的是( )
| A.T2>T1,正反应放热,L是液体 |
| B.P2<P1,正反应吸热,L是固体 |
| C.T2<T1,正反应放热,L是气体 |
| D.P2>P1,正反应吸热,L是气体 |
氢气既是最理想的能源又是重要的化工原料,用甲烷制氢气是一种廉价的制氢方法。有关的热化学方程式如下: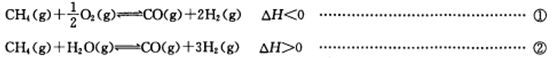
下列说法不正确的是
| A.当反应①中v(CH4)正=v(CO)逆时,表明该反应达平衡状态 |
| B.其他条件不变时,增大体系压强,反应①、②中甲烷的转化率均减小 |
| C.使用高效催化剂可以加快反应速率,同时提高CH4的转化率 |
| D.同一容器内同时发生反应①与②时,容器内温度可能保持不变 |
对于反应N2(g)+3H2(g) 2NH3(g) △H=-92kJ/mol,若只改变下列一个条件,一定能增大正反应速率且使平衡向正反应方向移动的是( )
2NH3(g) △H=-92kJ/mol,若只改变下列一个条件,一定能增大正反应速率且使平衡向正反应方向移动的是( )
| A.升高温度 | B.增大容器体积 |
| C.降低c(NH3) | D.将三种物质浓度均增大到原来的2倍 |
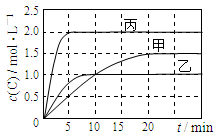
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
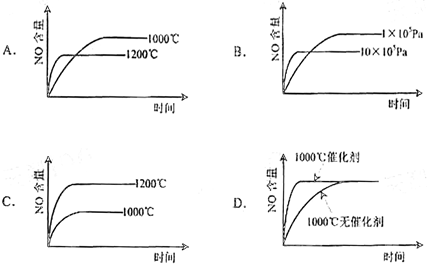
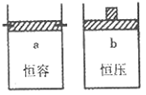
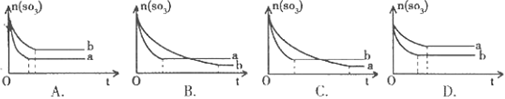
 2SO2(g)+O2(g),两容器中三氧化硫物质的量随时间(t)变化的示意图为
2SO2(g)+O2(g),两容器中三氧化硫物质的量随时间(t)变化的示意图为