题目内容
在密闭容器中进行下列反应:M(g)+N(g) R(g)+2 L( ?),反应符合下图。下列叙述正确的是( )
R(g)+2 L( ?),反应符合下图。下列叙述正确的是( )
| A.T2>T1,正反应放热,L是液体 |
| B.P2<P1,正反应吸热,L是固体 |
| C.T2<T1,正反应放热,L是气体 |
| D.P2>P1,正反应吸热,L是气体 |
C
解析试题分析:由图象可知,温度为T2时,根据到达平衡的时间可知P2>P1,且压强越大,R的含量越低,说明平衡向逆反应方向移动,正反应为气体体积增大的反应,故L为气体;压强为P2时,根据到达平衡的时间可知T1>T2,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应;A.由上述分析可知,T2<T1,正反应放热,L是气体,A错误;B.由上述分析可知,P2>P1,正反应放热,L是气体,B错误;C.由上述分析可知,T2<T1,正反应放热,L是气体,C正确;D.由上述分析可知,P2>P1,正反应放热,L是气体,D错误;选C。
考点:体积百分含量随温度、压强变化曲线

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案用铁片与0.1mol/L硫酸反应制氢气时,下列措施不能使氢气生成速率加大的是
| A.改用98%浓硫酸 | B.加热 |
| C.改用2mol/L硫酸 | D.把铁片换成铁粉 |
一定温度下,可逆反应 A2(g)+3B2(g)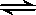 2AB3(g) 达到平衡的标志是
2AB3(g) 达到平衡的标志是
| A.容器内每减少1mol A2,同时生成2mol AB3 |
| B.容器内每减少1mol A2,同时生成3mol B2 |
| C.容器内A2、B2、AB3的物质的量之比为1:3:2 |
| D.容器内A2、B2、AB3的物质的量浓度相等 |
在容积恒定的密闭容器中,一定量的SO2与1.1molO2发生反应: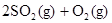
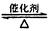
 。当气体的物质的量减少0.315mol时,反应达到平衡,SO2的平衡转化率是90%。下列说法正确的是
。当气体的物质的量减少0.315mol时,反应达到平衡,SO2的平衡转化率是90%。下列说法正确的是
| A.相同条件下,平衡时若充入稀有气体,SO2的转化率增大 |
| B.反应开始时,向容器中通入的SO2的物质的量是0.7mol |
| C.保持其他条件不变,仅降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| D.保持其他条件不变,仅缩小容器体积,反应达到平衡时容器中有1.485mol气体 |
对于可逆反应mA(g)+nB(g) pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ-t图象如下图。则如下关系正确的为
pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ-t图象如下图。则如下关系正确的为
①a1=a2;②a1<a2;③b1=b2;④b1<b2;⑤t1>t2;⑥t1=t2;⑦两图中阴影部分面积相等;⑧右图阴影部分面积更大
| A.②④⑤⑦ | B.②④⑥⑧ | C.②③⑤⑦ | D.②③⑥⑤ |
一定条件下,C0与H2反应可生成乙醇:2CO+4H2? CH3CH20H+H20。下列关于该反应的说法错误的是
| A.增大CO的浓度能减小反应速率 |
| B.升高体系温度能增大反应速率 |
| C.使用合适的催化剂可增大反应速率 |
| D.若反应在密闭容器中进行,H2和C0不能全部转化为产物 |
工业上采用乙烯和水蒸气合成乙醇的原理为:CH2=CH2(g) + H2O(g)  CH3CH2OH(g)。下图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是( )
CH3CH2OH(g)。下图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是( )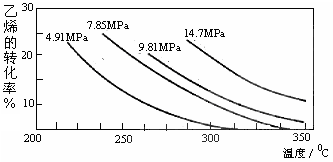
| A.该反应为吸热反应 |
| B.工业上采用7MPa左右,250~300℃,是综合考虑反应速率和乙醇的产率等因素的结果 |
| C.相同温度下,压强越大,乙烯的转化率越大,平衡常数越大 |
| D.给予足够的压强和适当的温度,可实现乙烯的转化率为 100% |
在容积均为500 mL的I、Ⅱ、Ⅲ三个密闭容器中分别充入l molN2和2.5 molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下发生反应N2(g)+3H2(g)2NH3(g)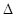 H<O。实验测得反应均进行到t min时N2的体积分数如图所示。下列说法正确的是
H<O。实验测得反应均进行到t min时N2的体积分数如图所示。下列说法正确的是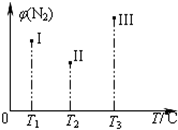
| A.当z,v(H2)=3v(N2)时,可以说明三个容器中的反应达平衡状态 |
| B.在t min时,一定达化学平衡状态的是Ⅱ和Ⅲ |
| C.在t min时,一定没有达化学平衡状态的是I |
| D.三个容器中的反应均达到平衡后,容器I中混合气体的平均相对分子质量最小 |
