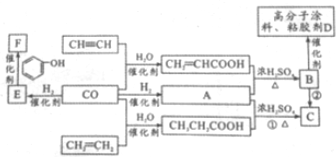
题目内容
6.实验室里需用道480mL0.1mol/L的硫酸铜溶液,以下配制溶液的操作正确的是( )| A. | 称取7.6g硫酸铜,加入500 mL的水 | B. | 称取8.0g硫酸铜,配成500mL溶液 | ||
| C. | 称取12.0g胆矾,配成500mL溶液 | D. | 称取12.5g胆矾,加入500mL水 |
分析 需要480mL溶液,实际只能配置500mL,根据n=c×V计算溶质的物质的量,配制硫酸铜溶液可以用硫酸铜,也可以用胆矾,根据m=n×M计算各自质量,配制溶液时注意水的体积不等于溶液的体积.
解答 解:需要480mL溶液,实际只能配置500mL,配制500mL 0.100mol•L-1的CuSO4溶液,溶质的物质的量为:n=c×V=0.5L×0.100mol/L=0.0500mol,需要溶质的质量为:m(CuSO4)=0.05mol×160g/mol=8.0g,
或m(CuSO4•5H20)=0.05mol×250g/mol=12.5g.
A.应称取8.0gCuSO4,配成500mL溶液,水的体积不等于溶液的体积,故A错误;
B.称取8.0gCuSO4,配成500mL溶液,溶液的浓度为 0.100mol•L-1,故B正确;
C.称取12.5g胆矾,配成500mL溶液,故C错误;
D.称取12.5g胆矾,配成500mL溶液,水的体积不等于溶液的体积,故D错误.
故选B.
点评 本题考查物质的量浓度的相关计算,题目难度不大,注意两点,一是配制硫酸铜溶液可以用硫酸铜,也可以用胆矾,二是注意水的体积不等于溶液的体积.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
9.下列反应中,水作为还原剂的是( )
| A. | Cl2+H2O=HCl+HClO | B. | 2Na2O2+2H2O=4NaOH+O2? | ||
| C. | 2F2+2H2O=4HF+O2? | D. | 2Na+4H2O=2NaOH+H2? |
10.原子序数依次增加的A、B、C、D、E、F六种常见元素中,A、B、C、D是短周期非金属元素,B、C、D同周期,E、F是第四周期的金属元素,F+的三个能层电子全充满.下表是主要化合价及原子半径数据:
请回答下列问题:
(1)B、C、D三种元素第一电离能数值由小到大的顺序是S<P<Cl(填元素符号);
(2)B的氢化物中心原子采取sp3杂化,空间构型是三角锥形,是极性分子(填“极性”或“非极性”);
(3)F2+与NH3形成配离子的化学式为[Cu(NH3)4]2+,F单质晶体晶胞是下图的③(填①、②、③或④);
(4)A,E两种元素形成晶体晶胞是图中的②(填①、②、③或④),A离子的配位数是4;若晶胞边长为apm(皮米),则A,E两种粒子的最近距离可表示为$\frac{\sqrt{3}}{4}$apm
(5)图5四条折线分别表示Ⅳ族、VA族、ⅥA族、VⅡA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线n(填n,m,x或y)
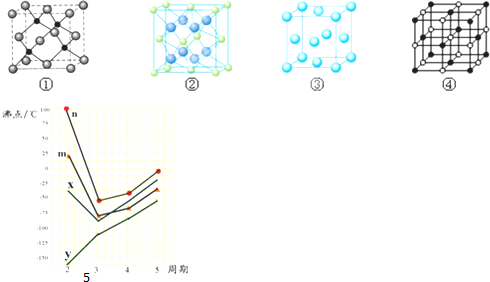
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3+5 | -2+6 | -1+7 | +2 | +1+2 |
| 原子半径nm | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |
(1)B、C、D三种元素第一电离能数值由小到大的顺序是S<P<Cl(填元素符号);
(2)B的氢化物中心原子采取sp3杂化,空间构型是三角锥形,是极性分子(填“极性”或“非极性”);
(3)F2+与NH3形成配离子的化学式为[Cu(NH3)4]2+,F单质晶体晶胞是下图的③(填①、②、③或④);
(4)A,E两种元素形成晶体晶胞是图中的②(填①、②、③或④),A离子的配位数是4;若晶胞边长为apm(皮米),则A,E两种粒子的最近距离可表示为$\frac{\sqrt{3}}{4}$apm
(5)图5四条折线分别表示Ⅳ族、VA族、ⅥA族、VⅡA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线n(填n,m,x或y)

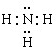 ,B的结构式为
,B的结构式为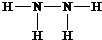 .
.
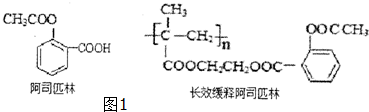
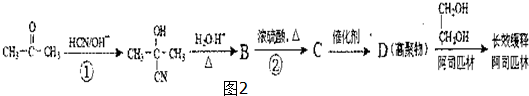
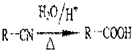 ,回答问题:
,回答问题: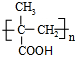 .
.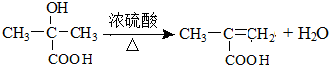 .
.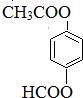 (只写一种).
(只写一种).