��Ŀ����
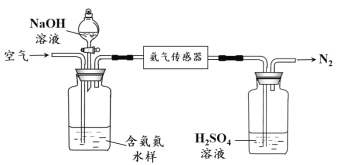
����Ŀ��ij�о���ѧϰС����̽������ɫ����������ˮ��Ӧ�Ƿų�����������������ʱ�������ͼ��ʾ��ʵ��װ�á�

��С�Թ������1g����ɫ�������ƣ���С�Թ����ڴ�֧�ܵ��Թ��ڡ���U�ι��ڼ���������īˮ����T�ι������У�ʹU�ι������ߵ�Һ�洦��ͬһˮƽ�档�ټн������У���ˮ����С�Թ��ڣ��ɹ۲쵽U�ι��Ҳ��Һ�������½�������Һ��������
��1���������Ƶĵ���ʽ__��
��2��д��������Ӧ�Ļ�ѧ����ʽ__��
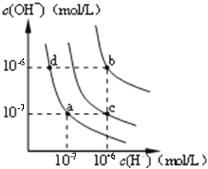
��3�����и�ͼ�У���ʾ����������ˮ��Ӧ��ͼ����_______��
A.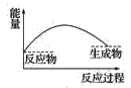 B.
B.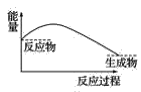
C.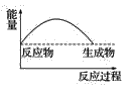 D.
D.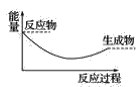
���𰸡�![]() 2Na2O2��2H2O=4NaOH��O2�� B
2Na2O2��2H2O=4NaOH��O2�� B
��������
�������������ӻ����������������������ԭ���γ�һ�Թ��õ��Ӷԣ�����������ˮ�ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����е��������������������������
��1���������������ӻ����������������������ԭ���γ�һ�Թ��õ��Ӷԣ��������Ƶĵ���ʽ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2���������ƺ�ˮ��Ӧ�����������ƺ���������Ӧ�Ļ�ѧ����ʽ2Na2O2��2H2O=4NaOH��O2�����ʴ�Ϊ��2Na2O2��2H2O=4NaOH��O2����
��3������������ˮ�ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����е����������������������������ѡB���ʴ�Ϊ��B��

 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�����Ŀ��W��X��Y��Z��M��E��Q��Ϊϡ��������Ķ�����Ԫ�أ�����ԭ��������������X��������������W��4����Z��E��������ϼ���ͬ��X��M�����ڱ���λ����ͼ��
X | ||
M | E |
��1��Y�����ڱ��е�λ��Ϊ________��Q��Ԫ������Ϊ_______��
��2��X�����������ĵ���ʽΪ____________________��Y��W�γɵ�������ӵĵ���ʽΪ_________________��
��3������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�________��
��4��X��E������������ˮ���ﷴӦ�Ļ�ѧ��ӦʽΪ___________________________��
��5��������ʵ��˵��ZԪ�صķǽ����Ա�EԪ�صķǽ�����ǿ����________
��Z������E�ļ��⻯�����Һ��Ӧ����Һ�����
����������ԭ��Ӧ�У�1mol Z���ʱ�1mol E���ʵõ��Ӷ�
��Z��E��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�߷ֽ��¶ȸ�
��6��M��Q��Ԫ�صĵ�������1mol M����ۻ�����ָ������£�����687kJ����֪�û�������ܷе�ֱ�Ϊ��69����58����д���÷�Ӧ���Ȼ�ѧ����ʽ��_________
��7��ͭ��һ��Ũ�ȵ����������Ļ��ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ���������������Ԫ���е�����Ԫ����ɡ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ����ᣬ����1L 2.2mol/L NaOH��Һ��1mol O2������������ķ���ʽ�Լ����ʵ����ֱ�Ϊ____________________�����ɵ�����ͭ�����ʵ���Ϊ____________
����Ŀ��������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��1����25�桢101kPa�£�1g�״���CH3OH��ȼ������CO2��Һ̬ˮʱ����22.68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ___��
��2��25�桢101kPa��������N2��O2��ȫ��Ӧ��ÿ����23gNO2��Ҫ����16.95kJ����___��
��3��25�桢101kPa��֪��1mol H��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ___��
��4���״�������Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϡ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ��������ºϳɼ״�����������Ҫ��Ӧ���£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��H2
CH3OH��g��+H2O(g) ��H2
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3
CO(g)+H2O(g) ��H3
�ش��������⣺
��֪��Ӧ������صĻ�ѧ�������������£�
��ѧ�� | H��H | C��O | C | H��O | C��H |
E/��kJ��mol-1�� | 436 | 343 | 1076 | 465 | 413 |
�ɴ˼�����H1=___kJ��mol-1����֪��H2=-58kJ��mol-1������H3=___kJ��mol-1��
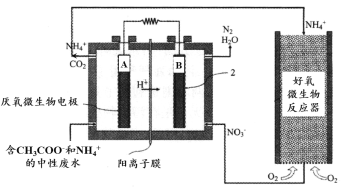
����Ŀ��ijͬѧ��ʵ�����н�������ʵ�飺
��� | �� | �� | �� |
ʵ�� |
|
|
|
���� | û�����Ա仯����Һ��Ϊ��ɫ | �г������ɣ���ҺΪ����ɫ | ����ɫ���ݲ��� |
���½��۲���ȷ���ǣ� ��
A.���������Ա仯��˵������Һ����Ӧ
B.���еİ�ɫ����ΪBaSO4
C.���з����ķ�Ӧ�����ӷ�Ӧ
D.���з�����Ӧ�����ӷ���ʽΪ2H����Zn��Zn2����H2��