题目内容
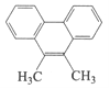
【题目】有机化合物9,10-二甲基菲的结构如图所示,下列关于该物质的说法正确的是
A. 该物质分子式为C16H12
B. 该物质与甲苯互为同系物
C. 该物质能与溴水发生取代反应和加成反应
D. 该物质苯环上七氯代物的同分异构体有4种
【答案】D
【解析】A. 根据结构简式可判断该物质分子式为C16H12,A错误;B. 该物质与甲苯的结构不相似,不能互为同系物,B错误;C. 该物质能与溴水发生取代反应,不存在碳碳双键,不能发生加成反应,C错误;D. 有机化合物9,10-二甲基菲的苯环上有8个氢原子,所以苯环上七氯代物的同分异构体和一氯代物的同分异构体数目是一样的,由于结构对称,一氯代物的同分异构体数目是4,所以苯环上七氯代物的同分异构体是4种,D正确,答案选D。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】甲酸乙酯为允许使用的食用香料,又称蚁酸乙酯,有辛辣的刺激味和菠萝样的果香香气,还有强烈朗姆酒似香气,并略带苦味。
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点如下
试剂 | 乙醚 | 乙醇 | 甲酸 | 甲酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 100.5 | 54.4 |
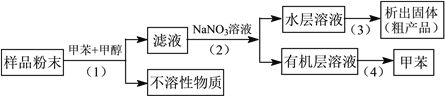
(1)制备粗品
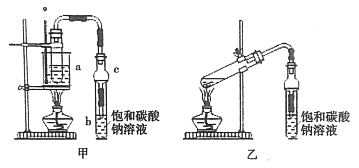
将4mL乙醇、3mL甲酸和2mL浓硫酸加入试管a中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管b内得到甲酸乙酯的粗品。
①实验时,加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是__________;浓硫酸用量又不能过多,原因是_________。
②球形干燥管C的作用是__________。
③若用乙装置制备甲酸乙酯,其缺点有__________。
(2)制备精品
①反应结束后,从试管b中分离出甲酸乙酯粗品所用的主要仪器__________。
②从b中分离出的甲酸乙酯中常含有少量的乙醇、乙醚和水,应先加入无水氯化钙,除去______,然后再通过_________操作得到甲酸乙酯。
③某同学用装有饱和氢氧化钠的试管收集甲酸乙酯,几乎没有收集到产物。原因是______________(用化学方程式解释)。
【题目】己知A、B、C、D、E、F、G都是周期表中前四周期的元素,他们的原子序数依次增大。其中A原子的L层有2个未成对电子。D是电负性最大的元素,E与F同主族,E的二价阳离子与C的阴离子具有相同的电子层结构。G3+离子3d轨道电子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
⑴A、B、C的第一电离能由小到大的順序为_____________。D的核外有____种运动状态不同的电子。
⑵A的最简单氢化物属于______(填“极性分子”和“非极性分子”)。AH3+离子空间构型是________,其中心原子采取______杂化。
⑶G和M (质子数为25)两元素的部分电离能数据列于下表:
元素 | M | G | |
电离能 (kJmol-1) | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态G2+再失去一个电子难。其原因是____________;
⑷晶体熔点:EC____FC (填“ > ”、“<”或“=”),原因是_______________。
(5)H2S和C元素的一种氢化物(分子式为H2C2)的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
h2s | 187 | 202 | 2.6 |
H2C2 | 272 | 423 | 以任意比互溶 |
h2s和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因___________。
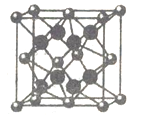
(6)FD2晶胞如图,已知DF核间距为a pm,则该晶体密度ρ=______g㎝-3(用带a、NA的算式表示,不必化简)