题目内容
在BaCl2溶液中通入足量SO2气体溶液仍澄清,此澄清溶液通入下列气体仍无明显现象的是( )
| A、NO2 |
| B、Cl2 |
| C、NH3 |
| D、CO2 |
考点:二氧化硫的化学性质
专题:氧族元素
分析:将SO2气体通入BaCl2溶液,未见沉淀生成,然后通入选项中气体,若有沉淀生成,气体应为强氧化性物质或碱性物质,可生成硫酸钡或亚硫酸钡沉淀,或是硫化氢,反之不能生成沉淀,以此解答.
解答:
解:A.NO2与水反应生成具有氧化性的硝酸,在溶液中将SO2氧化为SO42-离子,生成沉淀BaSO4,故A不选;
B.发生Cl2+SO2+2H2O═H2SO4+2HCl,H2SO4+BaCl2═BaSO4↓+2HCl,有沉淀生成,故B不选;
C.2NH3+SO2═(NH4)2S03,(NH4)2S03+BaCl2═BaSO3↓+2NH4Cl,有沉淀生成,故C不选;
D.二氧化碳和二氧化硫以及氯化钡均不反应,不会产生沉淀物,溶液一直澄清,故D选;
故选D.
B.发生Cl2+SO2+2H2O═H2SO4+2HCl,H2SO4+BaCl2═BaSO4↓+2HCl,有沉淀生成,故B不选;
C.2NH3+SO2═(NH4)2S03,(NH4)2S03+BaCl2═BaSO3↓+2NH4Cl,有沉淀生成,故C不选;
D.二氧化碳和二氧化硫以及氯化钡均不反应,不会产生沉淀物,溶液一直澄清,故D选;
故选D.
点评:本题考查物质的性质,综合考查元素化合物知识,为高频考点,把握二氧化硫的还原性及发生的氧化还原反应、复分解反应为解答的关键,题目难度不大.

练习册系列答案
相关题目
下列事实中,能说明HNO2是弱电解质的是( )
| A、用HNO2溶液做导电性实验,灯泡较暗 |
| B、HNO2是共价化合物 |
| C、HNO2溶液不与NaCl反应 |
| D、室温下,0.1mol?L-1 HNO2溶液的pH为2.15 |
在V mL Al2(SO4)3溶液中含有Al3+m g,取
mL该溶液用水稀释至4V mL,则SO42-物质的量浓度为( )
| V |
| 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
有人打算配制下列含有大量四种不同阴、阳离子的溶液,能成功的是( )
| A、H+、Ca2+、Cl-、HCO3- |
| B、Mg2+、Al3+、Cl-、SO42- |
| C、Na+、H+、NO3-、OH- |
| D、NH4+、Ag+、HCO3-、OH- |
白酒密封储存在地窖里,时间越长越香,形成这种香味效果的主要物质是( )
| A、醇类物质 | B、酯类物质 |
| C、酸类物质 | D、盐类物质 |
能将化学能转化为电能的装置(溶液均为稀硫酸)是( )
A、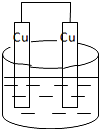 |
B、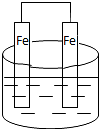 |
C、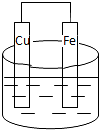 |
D、 |
下列化学反应属于加成反应的是( )
| A、油脂的皂化反应 |
| B、苯与浓硝酸、浓硫酸混合反应 |
| C、在一定条件下,苯与氢气的反应 |
| D、乙烯通入溴的四氯化碳溶液中的反应 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、1mol Cl2与足量Fe反应转移电子数一定为3NA |
| B、标准状况下,22.4L NH3中含有共价键的数目为NA |
| C、1.0L 1mol?L-1的硅酸钠水溶液中含有的氧原子数为3NA |
| D、4.6g Na完全转化成氧化钠和过氧化钠的混合物,混合物中阴离子总数为0.1NA |