题目内容
下列事实中,能说明HNO2是弱电解质的是( )
| A、用HNO2溶液做导电性实验,灯泡较暗 |
| B、HNO2是共价化合物 |
| C、HNO2溶液不与NaCl反应 |
| D、室温下,0.1mol?L-1 HNO2溶液的pH为2.15 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:只要证明HNO2在水溶液里部分电离,就能说明HNO2是弱电解质,据此分析解答.
解答:
解:A.用HNO2溶液做导电性实验,灯泡较暗,只能说明该溶液中自由移动的离子浓度较小,不能说明亚硝酸部分电离,所以不能证明亚硝酸是弱电解质,故A错误;
B.亚硝酸是共价化合物不能说明亚硝酸部分电离,所以不能证明亚硝酸是弱电解质,故B错误;
C.亚硝酸和氯化钠不反应,不能说明亚硝酸部分电离,则不能证明亚硝酸是弱电解质,故C错误;
D.常温下,0.1mol?L-1 HNO2溶液的pH为2.15,说明亚硝酸部分电离导致溶液中氢离子浓度小于亚硝酸浓度,则亚硝酸是弱电解质,故D正确;
故选D.
B.亚硝酸是共价化合物不能说明亚硝酸部分电离,所以不能证明亚硝酸是弱电解质,故B错误;
C.亚硝酸和氯化钠不反应,不能说明亚硝酸部分电离,则不能证明亚硝酸是弱电解质,故C错误;
D.常温下,0.1mol?L-1 HNO2溶液的pH为2.15,说明亚硝酸部分电离导致溶液中氢离子浓度小于亚硝酸浓度,则亚硝酸是弱电解质,故D正确;
故选D.
点评:本题考查了电解质强弱的判断,强弱电解质与是否是离子化合物无关、与物质的溶解性无关、与溶液导电能力无关,只与电离程度有关,为易错点.

练习册系列答案
相关题目
常温条件下,将SO2气体通入一定量的NaOH溶液中,所得溶液呈中性,关于该溶液判断正确的是( )
| A、该溶液中的溶质为NaHSO3 |
| B、溶液中的离子浓度最大的是Na+ |
| C、溶液中C(Na+)=C(SO32-)+C(HSO3-) |
| D、该溶液的溶质为NaHSO3和NaOH |
下列关于NaHCO3和Na2CO3的说法正确的是( )
①NaHCO3比Na2CO3稳定,便于长期保存; ②NaHCO3与酸的反应比Na2CO3快;
③鉴别NaHCO3与Na2CO3可以用Ca(OH)2 ④产生等质量的CO2,NaHCO3耗酸少.
①NaHCO3比Na2CO3稳定,便于长期保存; ②NaHCO3与酸的反应比Na2CO3快;
③鉴别NaHCO3与Na2CO3可以用Ca(OH)2 ④产生等质量的CO2,NaHCO3耗酸少.
| A、①③④ | B、①②③④ |
| C、①③ | D、②④ |
某电化学装置如图,下列说法正确的是( )
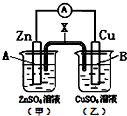

| A、若X是盐桥,则电子由B电极经外电路流向A电极 |
| B、若X是铜条,则A电极的电极反应式是:Zn2++2e-═Zn |
| C、若X是石墨条,则乙池溶液的pH会减小 |
| D、若X是锌条,则A电极的质量会减小 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| B、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| C、22.4L的CO2气体与1mol N2O所含的电子数均为22NA |
| D、T℃时,1L pH=6的纯水中,含OH-的数目为10-6NA |
 根据量子力学计算,氮化碳结构有五种,其中一种氮化碳硬度超过金刚石晶体,成为首届一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示.下列有关氮化碳的说法正确的是( )
根据量子力学计算,氮化碳结构有五种,其中一种氮化碳硬度超过金刚石晶体,成为首届一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示.下列有关氮化碳的说法正确的是( )| A、氮化碳属于分子晶体 |
| B、氮化碳的分了式为C3N4 |
| C、该晶体中的碳、氮原子核外都满足8电子稳定结构 |
| D、每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连 |
下列各组离子,在强酸性溶液中可以大量共存的是( )
| A、Na+、Ba2+、Cl-、SO32- |
| B、Na+、Ba2+、AlO2-、NO3- |
| C、NH4+、K+、Cl-、NO3- |
| D、Na+、K+、NO3-、SiO32- |
在BaCl2溶液中通入足量SO2气体溶液仍澄清,此澄清溶液通入下列气体仍无明显现象的是( )
| A、NO2 |
| B、Cl2 |
| C、NH3 |
| D、CO2 |
 Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题:
Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题: