题目内容
【题目】在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为 ( )
A. 0.1mol B. 0.5mol C. 0.15mol D. 0.25mol
【答案】B
【解析】由电荷守恒:1.5mol×1+0.5mol×2=1.5mol×1+n(SO42-)×2, n(SO42-)=0.5mol,选B。

【题目】肼(N2H4)是一种高能燃料,在生产和研究中用途广泛。化学小组同学在实验室中用过量NH3和NaC1O溶液反应制取N2H4(液)并探究其性质。回答下列问题:
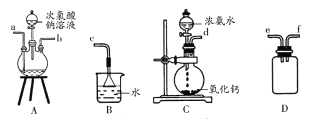
(1)肼的制备
①用上图装置制取肼,其连接顺序为________(按气流方向,用小写字母表示)。
②装置A中发生反应的化学方程式为_________________,装置D的作用是_______________。
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验:
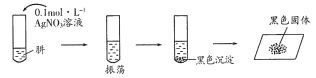
证明黑色沉淀已洗涤干净的操作是__________________________________。
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性。AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是_____________;
假设3:黑色固体可能是Ag和Ag2O。
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分。
实验编号 | 操作 | 现象 | 实验结论 |
1 | 取少量黑色固体于试管,__________ | 黑色固体不溶解 | 假设1成立 |
2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①________________ ②________________ | 假设3成立 |
根据实验现象,假设1成立,则N2H4与AgNO3溶液反应的离子方程式为____________。
【题目】下列图中的实验方案,能达到实验目的的是:( )
A | B | C | D | |
实验方案 |
|
|
|
|
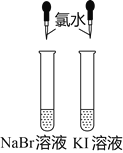
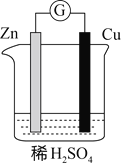
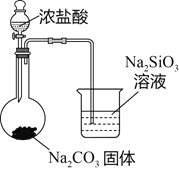
实验目的 | 验证FeCl3对H2O2分解反应有催化作用 | 验证单质氧化性: Cl2>Br2>I2 | 证实Zn与稀硫酸反应可以将化学能转化为电能 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
A. A B. B C. C D. D