题目内容
13.某气态烃1mol和2mol氯化氢完全加成反应,所得产物还能和8molCl2发生取代反应,最后得到一种只含碳和氯两种元素的化合物,则原有气态烃可能为( )| A. | CH≡CCH2CH2CH3 | B. | CH2CH2C≡CH | C. | CH2=CHCH3 | D. | CH≡CCH3 |
分析 1mol某烃最多能和2molHCl发生加成反应,则分子含有2个C=C键或1个C≡C,1mol该卤代烃能和8molCl2发生取代反应,生成只含碳元素和氯元素的化合物,卤代烃分子中含有8个H原子,其中2个H原子为烃与HCl发生加成反应引入,所以烃分子中含有6个H原子,据此结合选项判断.
解答 解:1mol某烃最多能和2molHCl发生加成反应,则分子含有2个C=C键或1个C≡C,1mol该卤代烃能和8molCl2发生取代反应,生成只含碳元素和氯元素的化合物,卤代烃分子中含有8个H原子,其中2个H原子为烃与HCl发生加成反应引入,所以烃分子中含有6个H原子,选项中只有CH2CH2C≡CH符合,
故选B.
点评 本题考查有机物分子式确定,侧重考查加成反应、取代反应,难度不大,有利于基础知识的巩固.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
3.氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )


| A. | Cl2+2NaBr═2NaCl+Br2 | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | D. | 4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O |
1.下列有关问题,与盐的水解有关的是( )
①配制硫酸铜溶液时加入少量硫酸
②铝盐和铁盐可作净水剂
③MgCl2溶液蒸干后灼烧得到MgO
④实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞.
①配制硫酸铜溶液时加入少量硫酸
②铝盐和铁盐可作净水剂
③MgCl2溶液蒸干后灼烧得到MgO
④实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞.
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ①②③④ |
18.在用锌、铜和稀H2SO4构成的原电池装置中,经过一段时间的工作后,下列说法正确的是( )
| A. | 锌是正极,铜上有气泡产生 | |
| B. | 电流方向是从锌到铜 | |
| C. | 电解液的pH保持不变 | |
| D. | 当导线中有1mol电子通过时,铜片上析出1 g H2 |
5.下列叙述正确的是( )
| A. | 在同温同压下,甲容器中的氧气(O2)和乙容器中的氨气(NH3)所含的原子个数相同,则甲、乙两容器中气体的体积之比为1:2 | |
| B. | 任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等 | |
| C. | 在标准状况时,20ml NH3与60ml N2所含的原子个数比为1:3 | |
| D. | 同温同压下,1L一氧化碳气体一定比1L氧气的质量小 |
2.下列物质中分子数最多的是( )
| A. | 标准状况下11.2LSO2 | B. | 3.01×1023个N2分子 | ||
| C. | 0.75mol H2SO4 | D. | 9g H2O |
3.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2 mol•L-1 的Na2SO4溶液中含有4NA个Na+ | |
| B. | 16克甲烷所含的电子数为10NA | |
| C. | 常温常压下,11.2L氧气中所含有的原子数为NA | |
| D. | NA个水分子的相对分子质量之和等于水的摩尔质量 |
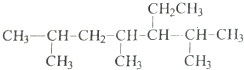 的系统命名是2,4,6-三甲基-3-乙基庚烷.
的系统命名是2,4,6-三甲基-3-乙基庚烷.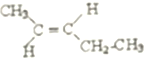 .
.