题目内容
16.写出下列反应的化学方程式,标出电子转移的方向和数目,并指出氯气在反应中表现出什么性质.(1)氢气在氯气中燃烧.
(2)氯气与石灰乳反应.
(3)铁在氯气中燃烧.
(4)适量的氯气与碘化钠溶液反应.
分析 (1)氢气在氯气中燃烧生成HCl,Cl元素的化合价降低;
(2)氯气与石灰乳反应生成氯化钙、次氯酸钙和水,Cl元素的化合价即升高又降低;
(3)铁在氯气中燃烧生成氯化铁,Cl元素的化合价降低;
(4)适量的氯气与碘化钠溶液反应反应生成单质碘和氯化钠,Cl元素的化合价降低.
解答 解:(1)氢气在氯气中燃烧生成HCl,Cl元素的化合价降低,氯气表现了氧化性,反应中转移2个电子,则标出电子转移的方向和数目为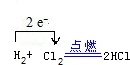 ,
,
故答案为:氧化性;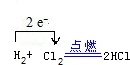 ;
;
(2)氯气与石灰乳反应生成氯化钙、次氯酸钙和水,Cl元素的化合价即升高又降低,氯气表现氧化性和还原性,反应中转移2个电子,则标出电子转移的方向和数目为 ;
;
故答案为:氧化性和还原性; ;
;
(3)铁在氯气中燃烧生成氯化铁,Cl元素的化合价降低,表现氧化性,反应中转移6个电子,则标出电子转移的方向和数目为 ;
;
故答案为:氧化性; ;
;
(4)适量的氯气与碘化钠溶液反应反应生成单质碘和氯化钠,Cl元素的化合价降低,表现氧化性,反应中转移了2个电子,则标出电子转移的方向和数目为 ;
;
故答案为:氧化性; .
.
点评 本题考查了氧化还原反应,侧重于电子转移和物质氧化性、还原性判断的考查,注意把握单线桥或双线桥表示氧化还原反应的方法,难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
6.下列有关硅和硅的化合物的叙述中正确的是( )
| A. | 二氧化硅是良好的半导体材料,可用于制造集成电路、晶体管器件和硅芯片等 | |
| B. | 硅的化学性质很稳定,常温下与酸、碱、盐等难以反应 | |
| C. | 硅酸俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| D. | 向含有少量酚酞的硅酸钠溶液中逐滴加入稀盐酸,边加边振荡,可以看到溶液红色逐渐消失 |
7.下列两种气体的分子数一定相等的是( )
| A. | 质量相等、密度不等的N2和C2H4 | B. | 相同压强、相同体积的CO和O2 | ||
| C. | 相同温度、相同体积的O2和N2 | D. | 质量相等的N2和CO2 |
4.下列描述或表达式正确的是( )
| A. | 反应MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O中1molMnO2被氧化转移2mol电子 | |
| B. | NaHSO4在熔融状态下的电离方程式为:NaHSO4═Na++HSO4- | |
| C. | 不溶于水的盐(CaCO3、BaSO4等)都是弱电解质 | |
| D. | 需要通电才可进行的有:电解、电泳、电离、电镀、电化腐蚀 |
10.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| C. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
 苯甲酸和苯甲酸钠均是食品防腐剂.某化学学习小组的同学们尝试用甲苯的氧化反应制备苯甲酸,实验过程如下:按图示装置,在圆底烧瓶中放入适量甲苯和水,在石棉网上加热至沸,从仪器X上口加入适量高锰酸钾,继续煮沸并间歇摇动烧瓶,直到甲苯层消失,回流液不再出现油珠时停止反应.
苯甲酸和苯甲酸钠均是食品防腐剂.某化学学习小组的同学们尝试用甲苯的氧化反应制备苯甲酸,实验过程如下:按图示装置,在圆底烧瓶中放入适量甲苯和水,在石棉网上加热至沸,从仪器X上口加入适量高锰酸钾,继续煮沸并间歇摇动烧瓶,直到甲苯层消失,回流液不再出现油珠时停止反应.
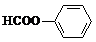 +2NaOH-→HCOONa+
+2NaOH-→HCOONa+ +H2O.
+H2O.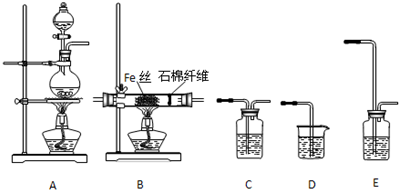
 ),乳酸在微生物作用下分解为CO2和H2O.
),乳酸在微生物作用下分解为CO2和H2O.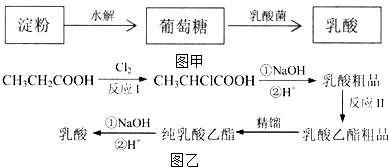
 乳酸在一定条件下发生反应得到聚乳酸的化学方程式是n
乳酸在一定条件下发生反应得到聚乳酸的化学方程式是n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +(n-1)H2O.
+(n-1)H2O.