题目内容
15.PNA是一种具有良好的热稳定性、耐腐蚀性和抗水性的高分子化合物,常用作增塑剂,其合成路线如图所示:
已知:①R1CH=CHR2$\stackrel{KMnO_{4}/H+}{→}$R1COOH+R2COOH (R1、R2代表烃基)
②
 (R1、R2、R3代表烃基或氢原子)
(R1、R2、R3代表烃基或氢原子)请回答:
(1)A分子中只有一个氯原子,A→B的化学方程式是
 .
.(2)C含有的官能团名称是羧基.
(3)D能发生银镜反应,且分子中有支链,D的结构简式是
 .
.(4)E→F的反应类型是加成反应(或还原反应).
(5)E的结构简式是
 .若一次取样,检验E中所含官能团,按使用顺序加入试剂为Na、银氨溶液(或新制的Cu(OH)2悬浊液).
.若一次取样,检验E中所含官能团,按使用顺序加入试剂为Na、银氨溶液(或新制的Cu(OH)2悬浊液).(6)C与F在一定条件下生成增塑剂PNA的反应的化学方程式是:
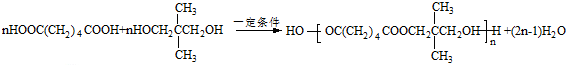 .
.(7)香豆素是一种重要的香料,与C具有相同的相对分子质量;14.6g香豆素完全燃烧生成39.6g CO2和5.4g H2O.
①香豆素的分子式是C9H6O2.
②写出所有符合下列条件的香豆素的同分异构体的结构简式
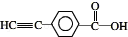
 .
.a.分子中含有
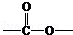 基团
基团 b.分子中除一个苯环外,无其他环状结构
c.苯环上的氢原子被氯原子取代,得到两种一氯代物.
分析 由合成图可知,环己烷与氯气光照下发生取代反应生成A,A分子中只有一个氯原子,则A为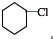 ,然后发生消去反应生成B为
,然后发生消去反应生成B为 ,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为
,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为 ,结合信息②可知,D与HCHO反应生成E为
,结合信息②可知,D与HCHO反应生成E为 ,E与氢气发生加成生成F为
,E与氢气发生加成生成F为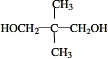 ,C与F发生酯化反应生成PNA为
,C与F发生酯化反应生成PNA为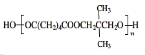 ,据此解答.
,据此解答.
解答 解:由合成图可知,环己烷与氯气光照下发生取代反应生成A,A分子中只有一个氯原子,则A为 ,然后发生消去反应生成B为
,然后发生消去反应生成B为 ,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为
,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为 ,结合信息②可知,D与HCHO反应生成E为
,结合信息②可知,D与HCHO反应生成E为 ,E与氢气发生加成生成F为
,E与氢气发生加成生成F为 ,C与F发生酯化反应生成PNA为
,C与F发生酯化反应生成PNA为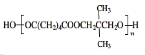 ,
,
(1)A为 ,然后发生消去反应生成B为
,然后发生消去反应生成B为 ,反应方程式为
,反应方程式为 ,
,
故答案为: ;
;
(2)C为HOOCCH2CH2CH2CH2COOH,官能团名称为羧基,故答案为:羧基;
(3)D能发生银镜反应,且分子中有支链,则D为 ,故答案为:
,故答案为: ;
;
(4)E与氢气发生加成生成F为 ,故答案为:加成反应(或还原反应);
,故答案为:加成反应(或还原反应);
(5)E为 ,含有羟基和醛基,若一次取样,检验E中所含官能团,需先用活泼金属Na检验羟基,再用银氨溶液(或新制的Cu(OH)2悬浊液)检验醛基,故答案为:
,含有羟基和醛基,若一次取样,检验E中所含官能团,需先用活泼金属Na检验羟基,再用银氨溶液(或新制的Cu(OH)2悬浊液)检验醛基,故答案为: ;Na、银氨溶液(或新制的Cu(OH)2悬浊液);
;Na、银氨溶液(或新制的Cu(OH)2悬浊液);
(6)由C和F合成PNA的化学方程式是: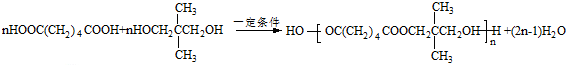 ,
,
故答案为: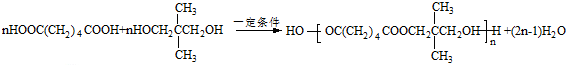 ;
;
(7)①香豆素是一种重要的香料,与C具有相同的相对分子质量,相对分子质量为146,14.6g香豆素完全燃烧生成39.6g CO2和5.4g H2O,即0.1mol香豆素燃烧生成0.9molCO2和0.3molH2O,再由质量守恒可知,含有氧原子的物质的量为$\frac{14.6g-0.9mol×12g/mol-0.6g}{16g/mol}$=0.2mol,所以香豆素的分子式是C9H6O2,故答案为:C9H6O2;
②香豆素的同分异构体符合a.分子中含有 基团;b.分子中除一个苯环外,无其他环状结构;c.苯环上的氢原子被氯原子取代,得到两种一氯代物,
基团;b.分子中除一个苯环外,无其他环状结构;c.苯环上的氢原子被氯原子取代,得到两种一氯代物,
则其同分异构体的结构简式为
 ,故答案为:
,故答案为:
 .
.
点评 本题考查有机物的推断与合成,注意根据有机物的结构和反应条件推断,需要学生对给予的信息进行利用,熟练掌握官能团的性质与转化,较好的考查学生自学能力与知识迁移运用,是有机题目常见题型,难度中等.

 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述反应可知氧化性HNO3>Fe3+>稀硫酸 | |
| C. | 上述过程中,会产生一种无色、难溶于水的气体 | |
| D. | 若通入的SO2完全反应,则通入的SO2和逸出的气体物质的量之比为1:1 |
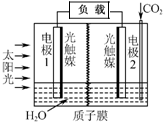 利用人工模拟光合作用合成甲酸的原理为:
利用人工模拟光合作用合成甲酸的原理为:太阳能光触媒2CO2+2H2O $→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
| A. | 电极1周围pH增大 | |
| B. | 电子由电极1经过负载流向电极2 | |
| C. | 电极2的反应式:CO2+2H++2e-=HCOOH | |
| D. | 该装置能将太阳能转化为化学能和电能 |
| A. | H2O+2F2═4HF+O2 | B. | H2O+3NO2═2HNO3+NO | ||
| C. | 3H2O+P2O5═2H3PO4 | D. | H2O+Si+2NaOH═2H2↑+Na2SiO3 |
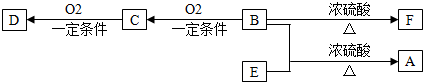
 Ⅰ、由生物质能通过绿色化学途径制取氢气是当前能源发展的一个重要方向.如图表示的是以CaO为吸收体,将生物质经与水蒸气反应制取H2的流程(生物质简写为C).
Ⅰ、由生物质能通过绿色化学途径制取氢气是当前能源发展的一个重要方向.如图表示的是以CaO为吸收体,将生物质经与水蒸气反应制取H2的流程(生物质简写为C).其中气化炉和燃烧炉中分别发生的主要反应如表所示:
| 气化炉 | 燃烧炉 |
| ①C(s)+H2O(g)?CO(g)+H2(g)△H=+131.6kJ•mol-1 ②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1 ③CaO(s)+CO2(g)?CaCO3(s)△H=-178.3kJ•mol-1 | ④C(s)+O2(g)═CO2(g) △H=-393.8kJ•mol-1 ⑤CaCO3(s)?CaO(s)+CO2(g) K |
(1)气化炉中的总反应为C(s)+2H2O(g)+CaO(s)═CaCO3(s)+2H2(g)△H=-87.9 kJ•mol-1.
(2)燃烧炉中反应⑤所需的能量由反应④提供.如果生成1mol CaO,至少需通入纯氧0.453mol.(留三位小数点)
(3)下表列出的是当只改变温度或压强时,反应⑤中CO2的浓度和CaCO3的残留率的变化.
 | 0 | 5 | 10 | 15 | 20 | 25 |
| T1 | 0 | 1.5 | 2.3 | 4.0 | 4.0 | 4.0 |
| T2 | 0 | 1.0 | 1.8 | 2.8 | 3.1 | 3.1 |
 | 0 | 5 | 10 | 15 | 20 | 25 |
| p1 | 1 | 0.90 | 0.83 | 0.75 | 0.75 | 0.75 |
| p2 | 1 | 0.58 | 0.35 | 0.31 | 0.30 | 0.30 |
Ⅱ、以熔融碳酸盐(Li2CO3)为电解质,一氧化碳-空气燃料电池的负极反应式为CO-2e-+CO32-=2CO2.在标准状况下,11.2L氧气参与反应,理论上转移的电子数为2NA(或1.204×1024).
 铜及其化台物在工业、农业、科技和日常生活中有广泛应用.
铜及其化台物在工业、农业、科技和日常生活中有广泛应用.