题目内容
19.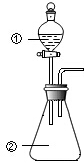 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( ) | 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.先发生盐酸与NaOH的反应;
B.常温下,Al遇浓硝酸发生钝化;
C.NaOH过量,开始不生成沉淀;
D.发生氧化还原反应.
解答 解:A.先发生盐酸与NaOH的反应,然后盐酸与碳酸钠反应生成碳酸氢钠,最后盐酸与碳酸氢钠反应生成气体,则现象不合理,故A错误;
B.常温下,Al遇浓硝酸发生钝化,则不能观察到红棕色气体,现象不合理,故B错误;
C.NaOH过量,开始不生成沉淀,反应生成偏铝酸钠和氯化钠,开始无现象,故C错误;
D.草酸与高锰酸钾发生氧化还原反应,溶液褪色,现象合理,故D正确;
故选D.
点评 本题考查物质的性质及实验装置的综合应用,为高频考点,为2015年高考真题,把握物质的性质、发生的反应、反应与现象的关系为解答的关键,侧重分析与实验能力的综合考查,综合性较强,题目难度中等.

练习册系列答案
相关题目
10.个体小煤矿经常发生瓦斯爆炸事故,造成多人伤亡,因此在矿井中,必须采取安全措施,如通风、严禁烟火等,而且要随时检查瓦斯的体积分数,如果空气中含甲烷5%~15%,运到明火会发生爆炸,发生最强烈爆炸时空气中甲烷所占的体积分数是( )
| A. | 5% | B. | 9.1% | C. | 10.5% | D. | 15% |
7.NH3及其盐都是重要的化工原料.
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为ACG.

(2)按图装置进行NH3性质实验.

①先打开旋塞1,B瓶中的现象是出现白烟,原因是A瓶压强比B瓶大,氯化氢进入B瓶与氨气反应生成氯化铵固体小颗粒形成白烟,稳定后,关闭旋塞1.
②再打开旋塞2,B瓶中的现象是烧瓶中的液体倒吸入B瓶,且紫色石蕊试液变红.
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响.
限选试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究温度对溶液中NH4Cl水解程度的影响.
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积).
③按实验序号1所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应的平衡转化率为$\frac{1{0}^{-Y}×0.1×53.5}{m}×100%$(只列出算式,忽略水自身电离的影响).
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为ACG.

(2)按图装置进行NH3性质实验.

①先打开旋塞1,B瓶中的现象是出现白烟,原因是A瓶压强比B瓶大,氯化氢进入B瓶与氨气反应生成氯化铵固体小颗粒形成白烟,稳定后,关闭旋塞1.
②再打开旋塞2,B瓶中的现象是烧瓶中的液体倒吸入B瓶,且紫色石蕊试液变红.
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响.
限选试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究温度对溶液中NH4Cl水解程度的影响.
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积).
| 物理量 实验序号 | V(溶液)/ml | … | |||
| 1 | 100 | … | |||
| 2 | 100 | … |
14.某研究小组将纯净的SO2气体通入0.1mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀.为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2;
(1)验证假设一
该小组设计实验验证了假设一,请在下表空白处填写相关实验现象.
(2)为深入研究该反应,该小组还测得上述两个实验中溶液pH随通入SO2体积的变化曲线如图.
实验1中溶液pH变小的原因是SO2溶于水后生成H2SO3;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2H2O+2NO3-=2NO+4H++3SO42-.
(3)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论.
(4)若假设二成立,请预测:在相同条件下,分别用足量的O2和KNO3氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反应后两溶液的pH前者小于(填“大于”或“小于”)后者,理由是反应的离子方程式表明,足量的O2和NO3-分别氧化相同的H2SO3,生成的H+的物质的量前者大于后者.
假设一:溶液中的NO3-
假设二:溶液中溶解的O2;
(1)验证假设一
该小组设计实验验证了假设一,请在下表空白处填写相关实验现象.
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25mL0.1mol•L-1BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体. | 无现象 | 假设一成立 |
| 实验2:在盛有不含O2的25mL0.1mol•L-1Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | 生成白色沉淀 |

实验1中溶液pH变小的原因是SO2溶于水后生成H2SO3;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2H2O+2NO3-=2NO+4H++3SO42-.
(3)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论.
| 实验步骤、预期现象和结论(不要求写具体操作过程): |
4.W、X、Y、Z均为的短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )
| A. | 单质的沸点:W>X | B. | 阴离子的还原性:W>Z | ||
| C. | 氧化物的水化物的酸性:Y<Z | D. | X与Y不能存在于同一离子化合物中 |
11.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下:

下列说法正确的是( )

下列说法正确的是( )
| A. | CO和O生成CO2是吸热反应 | |
| B. | 在该过程中,CO断键形成C和O | |
| C. | CO和O生成了具有极性共价键的CO2 | |
| D. | 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 |
8.下列说法正确的是( )
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7 | |
| C. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 | |
| D. | 0.1mol AgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
 (用电子式表示).
(用电子式表示).