题目内容
【题目】冬季下雪后,城市道路常使用融雪剂,其主要成分的 化学式为 XY2,X、Y 均为周期表前 20 号元素,其阳离子和阴离子电子层结构相同,且 1 mol XY2 含有 54 mol 电子。
(1)Y在周期表中的位置为_________,该融雪剂的化学式是________,该物质中化学键类型是________。
(2)元素 D、E 原子的最外层电子数均是其电子层数的2倍,D与Y相邻,则D的原子结构示意图是_____;D 与 E 能形成一种结构类似于 CO2 的三原子分子,且每个原子均达到了 8e-稳定结构,该分子的电子式为_______。
(3)元素Z的M层电子比L层少5个,Z与NaOH溶液反应的现象是_______,反应的离子方程式为_______。
【答案】第三周期第VIIA 族 CaCl2 离子键 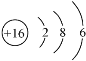
![]() 有气泡产生 2Al+2OH-+2H2O=2
有气泡产生 2Al+2OH-+2H2O=2![]() +3H2↑或2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
+3H2↑或2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
【解析】
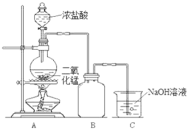
(1)融雪剂主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,含有相同的核外电子数,且1molXY2含有54mol电子,则阴、阳离子核外电子数为![]() =18,则为Ca2+、Cl-,XY2是CaCl2,X为Ca元素,Y为Cl元素。
=18,则为Ca2+、Cl-,XY2是CaCl2,X为Ca元素,Y为Cl元素。
(2)元素 D、E 原子的最外层电子数均是其电子层数的2倍,则分别为C和S,D与氯元素相邻,则D为硫元素,E为C元素。
(3)元素Z的M层电子比L层少5个,则其M层电子数为8-5=3,所以Z为Al元素。
(1)Y为Cl元素,位于元素周期表第三周期第VIIA 族;根据分析可知该融雪剂为CaCl2;氯化钙中只含钙离子和氯离子之间的离子键;
(2)D为S,S原子的结构示意图为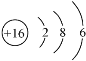 ;D 与 E 能形成一种结构类似于 CO2 的三原子分子,且每个原子均达到了 8e-稳定结构,该分子为CS2,与二氧化碳结构类似,其结构式为:S=C=S,电子式为
;D 与 E 能形成一种结构类似于 CO2 的三原子分子,且每个原子均达到了 8e-稳定结构,该分子为CS2,与二氧化碳结构类似,其结构式为:S=C=S,电子式为![]() ;
;
(3)Al可以与NaOH溶液反应生成氢气和偏铝酸钠(或四羟基合铝酸钠),所以可以看到有气泡生成,相应的离子方程式为2Al+2OHˉ+2H2O=2![]() +3H2↑或2Al+2OHˉ+6H2O=2[Al(OH)4]ˉ+3H2↑。
+3H2↑或2Al+2OHˉ+6H2O=2[Al(OH)4]ˉ+3H2↑。

 名校课堂系列答案
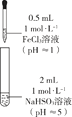
名校课堂系列答案【题目】某同学欲探究FeCl3溶液与NaHSO3溶液的反应,设计、完成实验并记录如下:
装置 | 反应时间 | 实验现象 |
| 0~1 min | 产生红褐色沉淀Fe(OH)3,有刺激性气味气体SO2逸出 |
1~30 min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 | |
30 min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
已知: Fe(OH)3+SO32-![]()
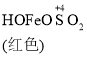
![]()
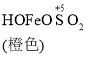
![]() Fe2++SO42-
Fe2++SO42-
下列有关反应速率和化学平衡说法不正确的是
A. 生成红色配合物的反应速率较快,红色配合物生成橙色配合物的速率较慢
B. 增大溶液中SO32-浓度可以加速红褐色沉淀Fe(OH)3迅速溶解
C. O2的作用下,橙色HOFeOSO2浓度下降,平衡![]() 不断正向移动
不断正向移动
D. 30min时,若向该无色溶液中滴加少量FeCl3溶液,无明显现象