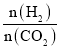题目内容
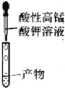
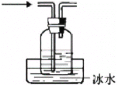
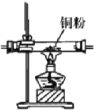
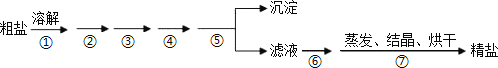
【题目】通过海水晾晒可得粗盐,粗盐除NaCl 外,还含有 MgCl2、CaCl2、Na2SO4 以及泥沙等杂质,粗盐精制的实验流程如下。下列说法不正确的是
A.在第①、⑦步中都运用了玻璃棒的搅拌作用
B.第⑤步操作是过滤
C.在第②③④⑥步通过加入化学试剂除杂,加入试剂顺序为:NaOH 溶液→Na2CO3 溶液→BaCl2 溶液→稀盐酸
D.除去MgCl2 的离子方程式为:Mg2++2OH=Mg(OH)2↓
【答案】C
【解析】
粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,除MgCl2用NaOH溶液,除CaCl2用Na2CO3,除Na2SO4用BaCl2溶液,但BaCl2的加入一定要在Na2CO3之前,加完三种试剂后,过滤,向滤液中加HCl溶液除去过量的Na2CO3,然后对所得溶液蒸发结晶即得精盐。
A.在第①步溶解时用玻璃棒搅拌,可以加速粗盐溶解,在第⑦步蒸发、结晶、烘干时用玻璃棒搅拌,使之受热均匀,避免产生飞溅,故A正确;
B.固液分离的操作是过滤,故B正确;
C.BaCl2溶液的加入一定要在Na2CO3溶液之前,否则过量的Ba2+无法除去,且一定要先过滤,再向滤液中加HCl,加入试剂正确顺序为NaOH 溶液→BaCl2 溶液→Na2CO3 溶液→过滤后在滤液中加稀盐酸,故C错误;
D.向粗盐中加NaOH除去MgCl2,其离子方程式为:Mg2++2OH-=Mg(OH)2↓,故D正确;
答案为C。

【题目】一定温度下,在三个体积均为2.0L的恒容密闭容器中分别加入一定量的X,发生反应:pX(g) ![]() Y(g)+Z(g),相关数据如下表所示:
Y(g)+Z(g),相关数据如下表所示:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
X(g) | Y(g) | Z(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | 0.160 | 0.160 |
Ⅲ | T | 0.20 | 0.090 | 0.090 |
回答下列问题:
(1)若容器Ⅰ中反应经10min达到平衡,则前10min内Y的平均反应速率v(Y)=___________。容器Ⅰ和容器Ⅱ中起始时X的反应速率v(X)Ⅰ___________v(X)Ⅱ(填“大于”“小于”或“等于”)。
(2)已知该正反应为放热反应,则T___________387(填“大于”或“小于”),判断理由是___________。
(3)反应方程式中X的化学计量数p的取值为___________,容器Ⅱ中X的平衡转化率为___________。若起始时向容器Ⅰ中充入0.1molX、0.15molY和0.10molZ,则反应将向___________ (填“正”或“逆”)反应方向进行,判断理由是_____________________________________________________。