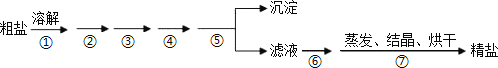
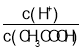题目内容
【题目】在两个固定体积均为1 L密闭容器中以不同的氢碳比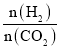 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是 ( )
C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是 ( )
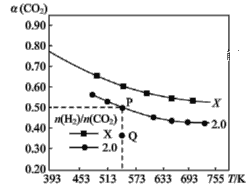
A.该反应在常温下不可能自发进行
B.氢碳比,X<2.0
C.若起始时CO2、H2浓度分别为0.5 mol·L-1、1.0 mol·L-1,则可得P点对应温度的平衡常数的值为512
D.向P点状态的容器中,按2∶4∶1∶4的比例再充入CO2、H2、C2H4、H2O,再次平衡后α(CO2)减小
【答案】C
【解析】
A.由图可知,随温度升高CO2的平衡转化率减小,说明升高温度,平衡逆向移动,则正反应为放热反应,故△H<0,反应的熵变△S<0,若△H-T△S<0,则需在低温下进行,故A错误;
B.氢碳比[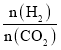 ]越大,二氧化碳的转化率越大,根据图像,氢碳比:X>2.0,故B错误;
]越大,二氧化碳的转化率越大,根据图像,氢碳比:X>2.0,故B错误;
C.由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比[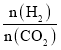 ]=2,起始时氢气为1mol/L、二氧化碳为0.5mol/L,则二氧化碳浓度变化量为0.25mol/L,则:
]=2,起始时氢气为1mol/L、二氧化碳为0.5mol/L,则二氧化碳浓度变化量为0.25mol/L,则:
2CO2(g)+6H2 (g)C2H4(g)+4H2O(g)
起始浓度(mol/L):0.5 1 0 0
变化浓度(mol/L):0.25 0.75 0.125 0.5
平衡浓度(mol/L):0.25 0.25 0.125 0.5
代入平衡常数表达式K=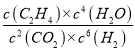 =
=![]() =512,故C正确;
=512,故C正确;
D.P点平衡时,CO2、H2、C2H4、H2O的浓度比值为2∶2∶1∶4,按2∶4∶1∶4的比例再充入CO2、H2、C2H4、H2O,增大了氢气的浓度,平衡正向移动,二氧化碳的转化率增大,即再次平衡后a(CO2)增大,故D错误;
故选C。

【题目】氮、磷、钾是农作物生长的必须营养元素,磷和钙都是促成骨骼和牙齿的钙化不可缺少的营养元素。回答下列问题:
(1)基态K的核外电子排布式为____________,基态N的价电子排布图为____________。
(2)元素的第一电离能:Ca________(填“>”或“<”)P。
(3)白磷P4在CS2中的溶解度________(填“大于”或“小于”)在水中的溶解度,N4是氮的一种新型单质,若N4分子结构类似于白磷P4,则N的杂化方式为________。
(4)下表是几种碳酸盐的热分解温度和阳离子半径:
碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 900 | 1172 | 1360 |
阳离子半径/pm | 99 | 112 | 135 |
根据上表数据分析碳酸钡分解温度最高的原因是_______________________
(5)常温下PCl5是一种白色晶体,晶体结构为氯化铯型,由A、B两种离子构成。已知A、B两种离子分别与CCl4、SF6互为等电子体,则A、B两种离子的符号分别为________、________。
(6)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。已知金属钙的晶胞为面心立方(如图)晶胞,晶胞边长为d pm;又知钙的密度为ρ g/cm3,则一个钙晶胞的质量为________(用d、ρ表示,下同)g,阿伏加德罗常数的值为______________(化成最简式)。