题目内容
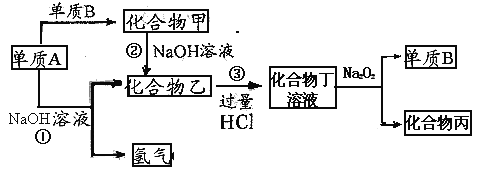
【题目】MnO2是一种重要的催化剂.某研究性学习小组设计了将粗MnO2(含有较多的 MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下: 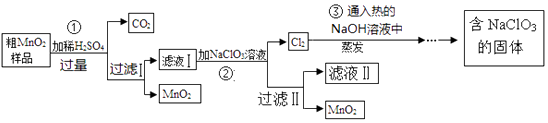
(1)检验操作A所得的MnO2是否洗涤干净的方法是 .
(2)第②步反应的离子反应方程式为 .
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、、、玻璃棒.
(4)上述流程中可用于循环使用的物质是(填化学式).
(5)MnO2不仅可作催化剂还可作氧化剂,写出1个用二氧化锰作氧化剂的化学反应方程式 .
(6)若粗MnO2样品的质量为24.28g,第①步反应后,经过滤得到18.35g MnO2 , 并收集到0.672LCO2(标准状况下),则样品中所含的MnO质量为g.
【答案】
(1)取最后一次洗涤液于试管中,滴加氯化钡溶液,若无浑浊现象出现,说明已洗涤干净
(2)5Mn2++2ClO3﹣+4H2O=5MnO2+Cl2↑+8H+
(3)酒精灯;蒸发皿
(4)NaClO3
(5)2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
(6)2.48
【解析】解:粗MnO2(含有较多的MnO和MnCO3)样品中加入过量的稀硫酸,由于MnO2不溶于硫酸,则样品中的MnO和MnCO3分别和硫酸反应生成可溶性的MnSO4 , 过滤得滤液Ⅰ为硫酸锰溶液,加入NaClO3发生反应为:5Mn2++2ClO3﹣+4H2O=5MnO2+Cl2↑+8H+ , 再过滤得到滤液Ⅱ和二氧化锰固体,而氯气与热的氢氧化钠反应生成氯酸钠方程式为:3Cl2+6NaOH=NaClO3+NaCl+3H2O;(1)检验过滤Ⅰ所得的MnO2是否洗涤干净的方法是取最后一次洗涤液于试管中,滴加氯化钡溶液,若无浑浊现象出现,说明已洗涤干净,所以答案是:取最后一次洗涤液于试管中,滴加氯化钡溶液,若无浑浊现象出现,说明已洗涤干净;(2)MnSO4要转化为MnO2 , 需失去电子,故需要加入NaClO3做氧化剂,依据得失电子守恒可以配平,所以反应的化学方程式是:5MnSO4+2NaClO3+4H2O=5MnO2+Cl2↑+Na2SO4+4H2SO4 , 因此反应的离子方程式是:5Mn2++2ClO3﹣+4H2O=5MnO2+Cl2↑+8H+ , 所以答案是:5Mn2++2ClO3﹣+4H2O=5MnO2+Cl2↑+8H+;(3)第③属于蒸发,所以所需的仪器有铁架台(含铁圈)、酒精灯、蒸发皿、玻璃棒,所以答案是:酒精灯、蒸发皿;(4)根据流程最终生成氯酸钠固体在第②步刚好也用到氯酸钠溶液,所以可用于循环使用的物质是NaClO3 , 所以答案是:NaClO3;(5)MnO2作催化剂,实验室分解氯酸钾制氧气的方程式为:2KClO3 ![]() 2KCl+3O2↑,所以答案是:2KClO3
2KCl+3O2↑,所以答案是:2KClO3 ![]() 2KCl+3O2↑;(6)根据质量守恒和化学方程式计算,CO2的物质的量为
2KCl+3O2↑;(6)根据质量守恒和化学方程式计算,CO2的物质的量为 ![]() =0.03mol,则MnCO3的物质的量为0.03mol,质量为115g/mol×0.03mol=3.45g,所以MnO的质量为24.28g﹣18.35g﹣3.45g=2.48g;所以答案是:2.48.
=0.03mol,则MnCO3的物质的量为0.03mol,质量为115g/mol×0.03mol=3.45g,所以MnO的质量为24.28g﹣18.35g﹣3.45g=2.48g;所以答案是:2.48.