题目内容
【题目】下列物质间可发生如下转化,
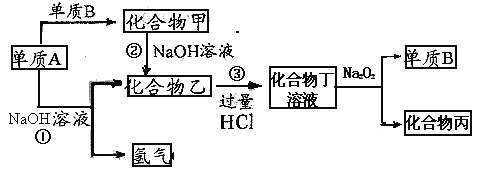
(1)写出化学式: 单质A ______,化合物丁 _______,化合物丙 _______,化合物乙 ___
(2)上述转化中用到了Na2O2 ,Na2O2是由______和钠离子两种离子构成的(填离子符号)。
(3)写出反应的化学方程式:
①______________ ② ______________
(4)写出Na2O2 与水反应的化学方程式: _________
【答案】 Al AlCl3 Al(OH)3 NaAlO2 O22- 2Al+2NaOH+2H2O===2NaAlO2+3H2↑ Al2O3 + 2NaOH===2NaAlO2+H2O 2Na2O2+2H2O=4NaOH+O2↑
【解析】试题分析:单质A能与氢氧化钠溶液反应放出氢气,所以单质A是铝;化合物乙是偏铝酸钠;偏铝酸钠与过量盐酸反应生成氯化铝,所以化合物丁是氯化铝;过氧化钠与水反应生成氢氧化钠和氧气,所以单质B是氧气,氯化铝与氢氧化钠反应生成氢氧化铝,化合物丙是氢氧化铝;铝与氧气反应生成氧化铝,所以化合物甲是氧化铝。
解析:根据以上分析,(1)单质A是Al,化合物丁是AlCl3,化合物丙是Al(OH)3,化合物乙 是NaAlO2。(2)Na2O2是离子化合物,由过氧根离子O22-和钠离子两种离子构成。
(3)①铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,方程式是2Al+2NaOH+2H2O===2NaAlO2+3H2↑
② 氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,化学方程式是:Al2O3 + 2NaOH===2NaAlO2+H2O;
(4)Na2O2 与水反应生成氢氧化钠和氧气,化学方程式是2Na2O2+2H2O=4NaOH+O2↑。

【题目】在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高.
物质 | A | B | C | D |
起始投料/mol | 2 | 2 | 3 | 0 |
该反应的平衡常数表达式为K= . 升高温度,平衡常数将(填“增大”“减小”或“不变”).