题目内容
下列物质中,属于合金的是( )
| A、金 | B、不锈钢 | C、金属铝 | D、铜 |
考点:金属与合金在性能上的主要差异
专题:元素及其化合物
分析:合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质,合金具有以下特点:①一定是混合物;②合金中至少有一种金属等.
解答:
解:A、金是纯净物,不属于合金,故A错误;
B、不锈钢是铁的合金,主要成分是铁,含有碳等杂质,故B正确;
C、金属铝是纯净物,不属于合金,故C错误;
D、铜是纯净物,不属于合金,故D错误;
故选B.
B、不锈钢是铁的合金,主要成分是铁,含有碳等杂质,故B正确;
C、金属铝是纯净物,不属于合金,故C错误;
D、铜是纯净物,不属于合金,故D错误;
故选B.
点评:本题难度不大,主要考查合金的特征,掌握合金的特征是正确解答本题的关键.

练习册系列答案
相关题目
MnO2和Zn是制造普通干电池的重要原料,工业上用软锰矿(主要成分MnO2)和闪锌矿(主要成分ZnS)来制取:
①将软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4═MnSO4+ZnSO4+S+2H2O;
②除去反应混合物中的不溶物;
③电解混合物:MnSO4+ZnSO4+2H2O
MnO2+Zn+2H2SO4
下列说法错误的是( )
①将软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4═MnSO4+ZnSO4+S+2H2O;
②除去反应混合物中的不溶物;
③电解混合物:MnSO4+ZnSO4+2H2O
| ||
下列说法错误的是( )
| A、干电池是一种将化学能转变为电能的装置 |
| B、步骤③电解时MnO2在阳极处生成,电极反应为:Mn2+-2e-+2H2O═MnO2+4H+ |
| C、步骤①每析出12.8g S沉淀,共转移0.8mol电子 |
| D、步骤③的反应也可以设计成原电池 |
已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W与Z、X和Y分别同主族,Y、Z同周期.Z能与X形成两种常见的离子化合物,离子个数比均为2:1.下列说法错误的是( )
| A、Y、Z、X、W的原子序数依次减小 |
| B、W与X可形成既含极性共价键又含非极性共价键的化合物 |
| C、由W、X、Y、Z四种元素组成的常见化合物一定显酸性 |
| D、X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
把镁带投入盛有盐酸的敞口容器里,下列因素对反应速率有影响的是( )
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度.
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度.
| A、①② | B、③④ |
| C、①②③④ | D、①②③ |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、9g D2O中含有的电子数为5NA |
| B、92g NO2和N2O4混合气体中含有原子数为6NA |
| C、1mol C3H8分子中共价键总数为8NA |
| D、65g Zn全部溶解在一定浓度的硝酸溶液中,有NO生成,则转移的电子数为NA |
下列各组原子序数表示的两种元素中,能够形成共价化合物的是( )
| A、11与17 | B、11与10 |
| C、1与17 | D、1与8 |
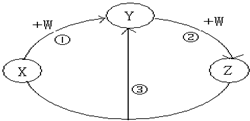 X、Y、Z、W都是中学化学常见的物质,其中X、Y、Z均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请按要求回答下列问题:
X、Y、Z、W都是中学化学常见的物质,其中X、Y、Z均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请按要求回答下列问题: