题目内容
把镁带投入盛有盐酸的敞口容器里,下列因素对反应速率有影响的是( )
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度.
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度.
| A、①② | B、③④ |
| C、①②③④ | D、①②③ |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:镁带投入盛有盐酸的敞口容器里,发生Mg与氢离子的反应,则改变氢离子浓度、Mg的接触面积、反应温度等均影响反应速率,以此来解答.
解答:
解:镁带投入盛有盐酸的敞口容器里,发生Mg与氢离子的反应,
①盐酸的浓度改变,氢离子浓度改变,则反应速率变化;
②镁带的表面积越大,反应速率越大;
③溶液的温度高,反应速率就大,改变温度,反应速率变化;
④氯离子实际不参加反应,则改变氯离子的浓度,反应速率无影响,
故选D.
①盐酸的浓度改变,氢离子浓度改变,则反应速率变化;
②镁带的表面积越大,反应速率越大;
③溶液的温度高,反应速率就大,改变温度,反应速率变化;
④氯离子实际不参加反应,则改变氯离子的浓度,反应速率无影响,
故选D.
点评:本题考查影响化学反应速率的因素,明确发生的反应实质及常见的影响反应速率的因素为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
常温下,0.1mol?L-1 NH4HCO3溶液的pH=7.8,该溶液中微粒浓度间关系正确的是( )
| A、c(OH-)>c(H+) |
| B、c(HCO3-)>c(NH4+) |
| C、c(NH4+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(H2CO3)+c(H+)=c(CO32-)+2c(NH3?H2O)+c(OH-) |
下列气体中,可用排水法收集且对人体无毒害的是( )
| A、NH3 |
| B、Cl2 |
| C、NO |
| D、N2 |
几种短周期元素的原子半径及主要化合价如下表:下列说法正确的是( )
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -3 | -2 | |
| A、元素X和Q形成的化合物中不可能含有共价键 |
| B、Q2-比R3-更容易失去电子 |
| C、X、Z、R的最高价氧化物的水化物之间可两两相互反应 |
| D、M(OH)2的碱性比XOH的碱性强 |
关于反应2Fe3++Cu═2Fe2++Cu2+说法不正确的是( )
| A、该反应中Fe3+是氧化剂 |
| B、该反应中Cu被氧化了 |
| C、2mol Fe3+反应后共得到4NA个电子 |
| D、氧化产物与还原产物的物质的量之比为1:2 |
2014年4月10日,兰州发生自来水苯含量超标事件.苯是石油化工的基本原料,苯进入人体内,可在造血组织本身形成有血液毒性的代谢产物,被世界卫生组织认定为致癌物质.下列关于苯的叙述正确的是( )
| A、苯环是单、双键交替组成的平面环状结构 | |||
| B、苯和乙烯均能使酸性KMnO4溶液褪色 | |||
C、苯的硝化反应: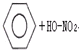
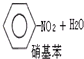 属于取代反应 属于取代反应 | |||
| D、苯跟溴水在催化剂作用下发生取代反应生成溴苯 |
下列物质中,属于合金的是( )
| A、金 | B、不锈钢 | C、金属铝 | D、铜 |

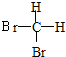 和
和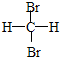 E.CH4和CH3(CH2)2CH3
E.CH4和CH3(CH2)2CH3