题目内容
【题目】下列反应的离子方程式正确的是( )
A.NaHCO3与足量Ca(OH)2的反应: 2HCO3-+Ca2++2OH-=CaCO![]() ↓+CO32-+2H2O
↓+CO32-+2H2O
B.少量Na投入冷水中;Na+2H2O=Na++OH-+H2↑
C.CuSO4与Ba(OH)2的反应: Cu2++ SO42-+Ba2++2OH![]() =Cu(OH)2↓+BaSO4↓
=Cu(OH)2↓+BaSO4↓
D.AlCl3溶液中加入足量氨水:Al3++4OH![]() =AlO2-+2H2O
=AlO2-+2H2O
【答案】C
【解析】
A.NaHCO3与足量Ca(OH)2的反应生成碳酸钙沉淀、氢氧化钠和水,反应的离子方程式为:HCO3-+Ca2++OH-=CaCO3↓+H2O,故A错误;
B.少量Na投入冷水中生成氢氧化钠和氢气,反应的离子方程式为;2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.CuSO4与Ba(OH)2的反应生成硫酸钡和氢氧化铜沉淀,反应的离子方程式为:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓,故C正确;
D.AlCl3溶液中加入足量氨水生成氢氧化铝沉淀和氯化铵,氨水不能溶解生成的氢氧化铝,反应的离子方程式为:Al3++3NH3H2O=Al(OH)3↓+3NH4+,故D错误;
故选C。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案【题目】Ⅰ.实验室制得气体中常含有杂质,影响其性质检验。下图A为除杂装置,B为性质检验装置,完成下列表格:
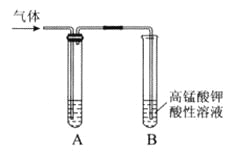
序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | _________ |
② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是________________。 | NaOH溶液 |
③ | 乙炔 | 电石与饱和食盐水反应 | _________ |
Ⅱ.为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
试管编号 | ① | ② | ③ |
实验操作 |
|
|
|
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是_____________________;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是________________;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_______________。