题目内容
【题目】(化学——选修5:有机化学基础)(15分)
有机化合物G是合成维生素类药物的中间体,其结构简式如图所示

G的合成路线如下图所示:

其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:
请回答下列问题:
(1)G的分子式是 ,G中官能团的名称是 ;
(2)第②步反应的化学方程式是 ;
(3)B的名称(系统命名)是 ;
(4)第②~⑥步反应中属于取代反应的有 (填步骤编号);
(5)第④步反应的化学方程式是 ;
(6)写出同时满足下列条件的E的所有同分异构体的结构简式 。
①只含一种官能团;②链状结构且无-O-O-;③核磁共振氢谱只有2种峰。
【答案】(1)C6H10O3;酯基和羟基 (2)(CH3)2CH CH2Br+NaOH![]() (CH3)2CH CH2OH+NaBr
(CH3)2CH CH2OH+NaBr
(3):2-甲基-1-丙醇 (4)②⑤ (5)
(6)CH3COOCH2CH2OOCCH3、CH3CH2OOCCOOCH2CH3、CH3OOCCH2CH2COOCH3
【解析】
根据反应③的产物可知A为![]() ,反应③为醇的氧化,根据G推知F为
,反应③为醇的氧化,根据G推知F为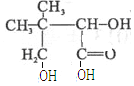 ,结合已知和反应⑤有乙醇产生推得C为
,结合已知和反应⑤有乙醇产生推得C为![]() ,反应④类似所给已知反应,则E为
,反应④类似所给已知反应,则E为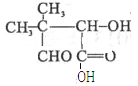 ,根据E的结构可知它含三种官能团,而它的同分异构体含一种官能团,可能是羧基或酯基,只有2中氢,应该有对称结构,有如下几种:CH3COOCH2CH2OOCCH3、CH3OOCCH2CH2COOCH3、CH3CH2OOCCOOCH2CH3
,根据E的结构可知它含三种官能团,而它的同分异构体含一种官能团,可能是羧基或酯基,只有2中氢,应该有对称结构,有如下几种:CH3COOCH2CH2OOCCH3、CH3OOCCH2CH2COOCH3、CH3CH2OOCCOOCH2CH3

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目









