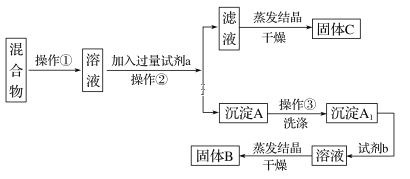
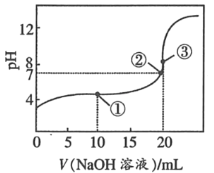
题目内容
【题目】M表示摩尔质量,NA表示阿伏加德罗常数,Vm表示气体摩尔体积,ω表示溶质的质量分数,ρ(单位为gcm-3)表示溶液的密度。下列说法中不正确的是( )
A.根据摩尔质量和阿伏加德罗常数可以计算得出某气体分子的质量:![]()
B.根据气体摩尔体积和阿伏加德罗常数可以计算得出该条件下某气体分子的大小:![]()
C.根据摩尔质量和气体摩尔体积可以计算得出该条件下某气体的密度:![]()
D.根据溶质的质量分数、摩尔质量和溶液的密度可以计算出某溶液的物质的量浓度:![]()
【答案】B
【解析】
A.1mol气体的质量为Mg,其中含有的分子数目为NA,则该气体分子的质量m(分子)=![]() g,A正确;
g,A正确;
B.气体分子在很大的空间运动,分子之间的间隔很大,因此不能根据气体摩尔体积和阿伏加德罗常数计算出该条件下某气体分子的大小,B错误;
C.根据密度公式,可得气体的密度ρ=![]() ,C正确;
,C正确;
D.根据溶液的物质的量浓度定义可知:单位体积的溶液中所含有的溶质的物质的量为溶液的物质的量浓度,则溶液的物质的量浓度c=![]() ,D正确;
,D正确;
故合理选项是B。

【题目】利用钛白粉厂废酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)制备过二硫酸铵[(NH4)2S2O8],同时回收TiO(OH)2的简要流程如下: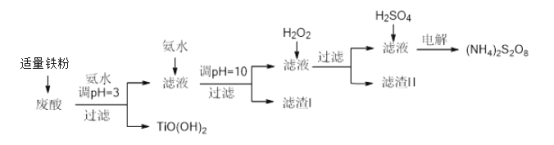
已知:i.部分离子完全生成氢氧化物沉淀的pH:
金属离子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
开始沉淀的PH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7时,Fe2+部分生成Fe(II)氨络离子[Fe(NH3)2]2+。
请回答下列问题:
(1)加入适量铁的作用是______________________________________。
(2)生成TiO(OH)2的化学方程式是________________________________。
(3)滤渣I、滤渣Ⅱ中均含有的物质的化学式是___________________________。
(4)加入H2O2的目的是氧化除掉Fe(II)氨络离子[Fe(NH3)2]2+,配平下列离子方程式:
2[Fe(NH3)2]2+ +____________+4H2O +H2O2 =___________ + 4NH3·H2O 。
(5)常温下,电解液中含硫微粒主要存在形式与pH的关系如下图所示。
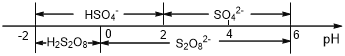
在阳极放电的离子主要为HSO4-,阳极区电解质溶液的pH范围为___________________________________
(6)已知Ksp[Al(OH)3]=3.2×10-34 ,当pH=10 时,求溶液中c(Al3+)=______________
(7)25℃,pH=3的(NH4)2SO4溶液中,计算2c(SO42-)- c(NH4+) =_______mol/L(列式即可)。