题目内容
【题目】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液。下列说法正确的是( )
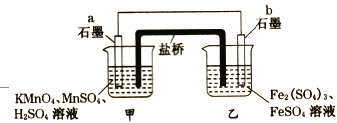
A. a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O
B. 外电路电子的流向是从a到b
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. b电极上发生还原反应
【答案】A
【解析】试题分析:A、总电极反应式:2MnO4-+10Fe2++16H+=2Mn2++10Fe3++8H2O,a极是正极得电子,电极反应式=总电极反应式-b极反应式,得出:2MnO4-+16H++10e-=2Mn2++8H2O,化简得:MnO4-+8H++5e-=Mn2++4H2O,A正确;B、根据A的分析,外电路电子流向是从b流向a,B错误;C、根据原电池的工作原理:阴离子向负极移动,阳离子向正极移动,SO42-向b极移动,C错误;D、根据原电池的工作原理:负极失电子,发生氧化反应,正极得电子发生还原反应,b极上电极反应式:Fe2+-e-=Fe3+,D错误,答案选A。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目