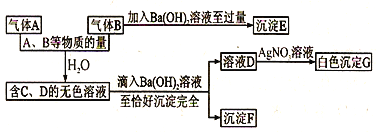
题目内容
【题目】将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.煤转化为水煤气的主要化学反应为:C+H2O(g) ![]() CO+H2 . C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
CO+H2 . C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
①C(s)+O2(g)=CO2(g)△H1=﹣393.5kJmol﹣1;
②H2(g)+ ![]() O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
③CO(g)+ ![]() O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
试回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式:
(2)比较反应热数据可知,1molCO(g)和1molH2(g)完全燃烧放出的热量之和,比1molC(s)完全燃烧放出的热量(填“多”或“少”).
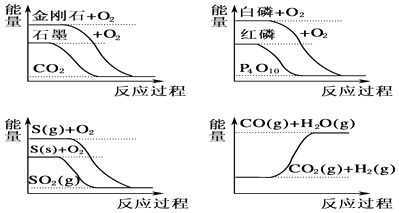
甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量”.乙同学根据盖斯定律作出了下列循环图
请你写出△H1、△H2、△H3、△H4之间存在的关系式 .
乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同.”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是 .
【答案】
(1)C(石墨,s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol
(2)多;△H1=△H2+△H3+△H4;乙;甲同学忽略了煤转化为水煤气要吸收热量
【解析】解:(1)①C(石墨,s)+O2(g)=CO2(g)△H=﹣393.5 kJ/mol,
②CO(g)+ ![]() O2(g)=CO2(g)△H=﹣283.0 kJ/mol,
O2(g)=CO2(g)△H=﹣283.0 kJ/mol,
③H2(g)+ ![]() O2(g)=H2O(g)△H=﹣242.0kJ/mol,
O2(g)=H2O(g)△H=﹣242.0kJ/mol,
根据盖斯定律,①﹣②﹣③得:C(石墨,s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol,
故答案为:C(石墨,s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol;
(2.)①C(s)+O2(g)=CO2(g)△H1=﹣393.5kJmol﹣1;
②H2(g)+ ![]() O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
③CO(g)+ ![]() O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
比较反应热数据可知,1molCO(g)和1molH2(g)完全燃烧放出的热量之和,比1molC(s)完全燃烧放出的热量多,
化学反应不管是一步完成还是分几步完成,其反应热是相同的;也就是说,化学反应的反应热只与反应的始态和终态有关,与反应途径无关.即如果一个反应可以分几步进行,则各步反应的反应热之和与该反应一步完成时的反应热相同;
△H1、△H2、△H3、△H4之间存在的关系式为:△H1=△H2+△H3+△H4;
依据盖斯定律可知,将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同,乙正确;
煤转化为水煤气要吸收热量,煤炭燃烧时加少量水,结合盖斯定律可知,煤炭燃烧放出相同的热量;
故答案为:多;△H1=△H2+△H3+△H4;乙;甲同学忽略了煤转化为水煤气要吸收热量.
(1)先根据燃烧热写出热化学方程式,然后根据盖斯定律来解答;(2)依据热化学方程式分析判断反应放出的热量;
根据盖斯定律:化学反应不管是一步完成还是分几步完成,其反应热是相同的;也就是说,化学反应的反应热只与反应的始态和终态有关,与反应途径无关.即如果一个反应可以分几步进行,则各步反应的反应热之和与该反应一步完成时的反应热相同;
根据煤转化为水煤气要吸收热量分析.

 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2 , 化学方程式如下:
2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)△H=﹣748kJ/mol
2CO2(g)+N2(g)△H=﹣748kJ/mol
为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | … |
c(NO)/molL﹣1 | 1.00×10﹣3 | 4.00×10﹣4 | 1.70×10﹣4 | 1.00×10﹣4 | 1.00×10﹣4 | … |
(1)前2s内的平均反应速率υ(N2)=(保留3位有效数字,下同);计算此温度下该反应的K= .
(2)达到平衡时,下列措施能提高NO转化率的是 . (填字母序号)
A.选用更有效的催化剂
B.降低反应体系的温度
C.充入氩气使容器内压强增大
D.充入CO使容器内压强增大
(3)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol;则CO的燃烧热为 .
(4)Ⅱ.臭氧也可用于处理NO.O3氧化NO结合水洗可产生HNO3和O2 , 每生成1mol的HNO3转移mol电子.
(5)O3可由电解稀硫酸制得,原理如图.图中阴极为(填“A”或“B”),阳极(惰性电极)的电极反应式为 .