题目内容
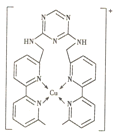
【题目】短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示:

请回答下列问题:
(1)D在元素周期表中的位置为___。
(2)A和C形成的一种摩尔质量为41g·mol-1的化合物,该化合物与盐酸反应能生成两种盐,其化学方程式为___。
(3)M为A的简单气态氮化物,其水溶液可作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为___。N为A的另一种氢化物,其相对分子质量比M大15,N为二元弱碱,在水中分步电离,并与M的电离方式相似,则N第一步电离的电离方程式为___,N与过量硫酸反应生成的酸式盐的化学式为___。
(4)下列事实能说明E元素的非金属性比D元素的非金属性强的是___ (填序号)。
①E的单质与D的气态氢化物的水溶液反应,生成淡黄色沉淀
②E与H2化合比D与H2化合更容易
③D与Fe化合时产物中Fe为+2价,E与Fe化合时产物中Fe为+3价
④等浓度的D和E的最高价含氧酸的水溶液中的c(H+):D>E
(5)D2E2分子中各原子最外层均满足8电子结构,则D2E2的电子式为___。
【答案】第三周期ⅥA族 AlN+4HCl=AlCl3+NH4Cl 2NH3+3H2O2=N2↑+6H2O或2NH3·H2O+3H2O2=N2↑+8H2O N2H4+H2O![]() N2H5++OH- N2H6(HSO4)2 ①②③
N2H5++OH- N2H6(HSO4)2 ①②③ ![]()
【解析】
由短周期元素A、B、C、D、E在元素周期表中的相对位置可知,A为N,B为O,C为Al,D为S,E为Cl。
A为N,B为O,C为Al,D为S,E为Cl。
(1)D为S,原子序数为16,位于周期表中的第三周期ⅥA族;
(2)A和C形成的一种摩尔质量为41g·mol-1的化合物,则该化合物为AlN。根据原子守恒,这两种盐分别为AlCl3和NH4Cl,其化学方程式为AlN+4HCl=AlCl3+NH4Cl;
(3)M为A的简单气态氢化物,为NH3,其水溶液为NH3·H2O,可作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为2NH3+3H2O2=N2+6H2O;N为A的另一种氢化物,其相对分子质量比M大15,则N为N2H4。N为二元弱碱,在水中分步电离,并与M的电离方式相似,则N第一步电离的电离方程式为N2H4+H2O![]() N2H5++OH-;N2H4作为二元弱碱,其阳离子为N2H62+,与过量硫酸反应生成的酸式盐为硫酸氢盐,阴离子为HSO4-,化学式为N2H6(HSO4)2;
N2H5++OH-;N2H4作为二元弱碱,其阳离子为N2H62+,与过量硫酸反应生成的酸式盐为硫酸氢盐,阴离子为HSO4-,化学式为N2H6(HSO4)2;
(4)①E的单质,即Cl2,与D的气态氢化物H2S的水溶液反应,生成淡黄色沉淀,发生反应Cl2+H2S=S↓+2HCl,Cl2置换出S,Cl2的氧化性大于S的氧化性,则可知非金属性Cl(E)大于S(D),正确;
②非金属元素的非金属性越强,与氢气化合越容易。Cl2与H2化合比S与H2化合更容易,可知非金属性Cl(E)大于S(D),正确;
③S与Fe化合时产物中Fe为+2价,Cl2与Fe化合时产物中Fe为+3价,Cl2得到电子能力强,可知非金属性Cl(E)大于S(D),正确;
④D的最高价含氧酸为H2SO4,E的最高价含氧酸为HClO4。同浓度下,H2SO4溶液中c(H+)大,是由于H2SO4为二元酸,HClO4为一元酸,且均为强酸,在溶液中完全电离,与它们的非金属性强弱无关,错误;
综上①②③符合题意;
(5)D2E2分子中各原子最外层均满足8电子结构,S达到稳定结构需要形成2对共用电子对,Cl达到稳定结构需要形成1对共用电子对,可知S2Cl2分子中S原子间共用1对电子,每个S原子与Cl原子共用一对电子,结构式为Cl-S-S-Cl,其电子式为![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 用乙酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性小于碳酸 |
B | 将MgCl2溶液加热蒸干,得到白色固体 | 固体为MgCl2 |
C | 向某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀 | 原溶液中有Fe2+ |
D | 向盛有1 mL 2 mol/L NaOH溶液的试管中滴入几滴0.1 mol/L MgCl2溶液,有白色沉淀生成;再加入几滴0.1 mol/L FeCl3溶液,有红褐色沉淀生成 | Ksp[Mg(OH)2] >Ksp[Fe(OH)3] |
A.AB.BC.CD.D
【题目】某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其它不溶于酸、碱的杂质。部分金属氢氧化物Ksp近似值如下表所示:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
现用含镍废催化剂制备NiSO4·7H2O晶体,其流程图如图:
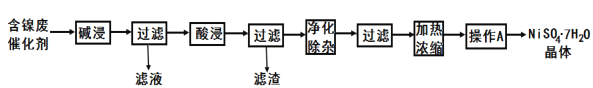
回答下列问题:
(1)滤液中的阴离子为_____。
(2)“酸浸”所使用的酸为_____。
(3)“净化除杂”是为了除铁,需加入H2O2溶液,溶液变成棕黄色,发生反应的离子方程式为__;一段时间后。溶液中有气泡出现,并放热.随后有红褐色沉淀生成。产生气泡的原因是__;然后调节pH就可使溶液中铁元素完全沉淀,若使其刚好沉淀完全(离子浓度为1.0×10-5mol/L),此时的pH=__(保留一位小数)
(4)“操作A”为_____、过滤、洗涤、干燥,即得产品。
(5)关于铁铝化合物的下列说法正确的是__(填序号)。
①配制FeCl3、AlCl3溶液时,均是先将固体FeCl3、AlCl3溶于较浓的盐酸,再用蒸馏水稀释到所需浓度
②FeCl2、FeCl3、Fe(OH)3均可以通过化合反应生成
③利用氯水和KSCN溶液可以检验FeCl3溶液中有无Fe2+
④加热蒸干Al2(SO4)3溶液残留固体的成分为Al2O3