题目内容
7.由乙醇制取乙二酸乙二酯时最简便的合成路线需经下列反应,①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应.合成乙二酸乙二酯的正确顺序是( )| A. | ①②③⑤⑥ | B. | ⑤②①③⑥ | C. | ⑥③①②⑤ | D. | ①②⑤③⑥ |
分析 制取乙二酸乙二酯,须先制备乙二酸和乙二醇,乙二酸可由乙二醇氧化而成;乙二醇可由乙烯与X2加成后再水解而得.
解答 解:发生反应如下: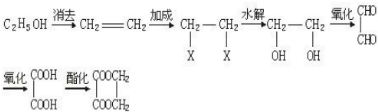 ,则发生反应为消去、加成、取代、氧化和酯化反应,故选B.
,则发生反应为消去、加成、取代、氧化和酯化反应,故选B.
点评 本题考查有机物制备,侧重考查学生知识运用能力,明确官能团及其性质关系是解本题关键,可以根据生成物确定反应物,熟练掌握常见有机反应类型及反应条件,题目难度中等.

练习册系列答案
相关题目
17.A、B、C、D、E是元素周期表前四周期中的五种常见元素,其相关信息如下表:
请回答下列问题
(1)C元素原子的价电子排布图是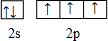
(2)E元素位于周期表ds区,E+离子的核外电子排布式是1s22s22p63s23p63d10
(3)CA3极易溶于水的主要原因是NH3与H2O分子间形成氢键C3-离子的中心原子采用sp杂化,C3-离子的空间构型是直线型
(4)A、C、E三种元素可形成〔E(CA3)4〕2+配离子,其中存在的化学键类型有①③(填序号,①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键)
(5)〔E(CA3)4〕2+可由E的硫酸盐溶液中通入过量CA3气体得到,写出该配离子的结构简式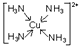 .
.
| 元素 | 相关信息 |
| A | A原子的1S轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2P轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
(1)C元素原子的价电子排布图是

(2)E元素位于周期表ds区,E+离子的核外电子排布式是1s22s22p63s23p63d10
(3)CA3极易溶于水的主要原因是NH3与H2O分子间形成氢键C3-离子的中心原子采用sp杂化,C3-离子的空间构型是直线型
(4)A、C、E三种元素可形成〔E(CA3)4〕2+配离子,其中存在的化学键类型有①③(填序号,①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键)
(5)〔E(CA3)4〕2+可由E的硫酸盐溶液中通入过量CA3气体得到,写出该配离子的结构简式
 .
.
18.根据下列事实所作的结论,正确的是( )
| 编号 | 事实 | 结论 |
| A | 甲、乙两种有机物具有相同相对分子质量和不同结构 | 甲和乙一定是同分异构体 |
| B | 质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 | 甲、乙两种分子中,H原子个数一定相同 |
| C | 不存在两种二氯甲烷 | CCl2F2一定只有一种 |
| D | 一种烃在足量的氧气中燃烧并通过浓硫酸后气体体积减少 | 减少的体积就是生成水蒸气的体积 |
| A. | A | B. | B | C. | C | D. | D |
15.下列关于钠、钾的说法正确的是( )
①钠的熔点比钾的熔点高
②钠和钾在空气中燃烧的产物都是过氧化物
③钠和钾性质活泼且都是短周期元素
④钠和钾的合金常用作原子反应堆的导热剂
①钠的熔点比钾的熔点高
②钠和钾在空气中燃烧的产物都是过氧化物
③钠和钾性质活泼且都是短周期元素
④钠和钾的合金常用作原子反应堆的导热剂
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
2.下列说法中正确的是( )
| A. | 离子化合物中可能含有共价键,共价化合物中可能含有离子键 | |
| B. | 一定条件下1 mol N2与3 mol H2在密闭容器中充分反应可生成2 mol NH3 | |
| C. | 铁质器件附有铜质配件,在接触处易生铁锈 | |
| D. | 非极性共价键只存在于双原子单质分子里 |
19.断肠草为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物,含有的毒素很多,从中分离出来的四种毒素的结构简式分别为:
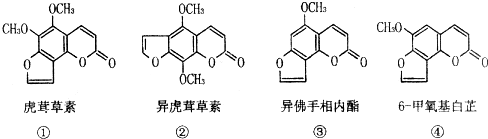
下列推断正确的是( )

下列推断正确的是( )
| A. | ①、②、③与④互为同分异构体 | |
| B. | ①、④互为同系物 | |
| C. | ③的分子式为C12H8O4 | |
| D. | 等物质的量②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少 |
16. 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表:
回答下列问题:
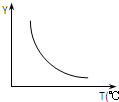
(1)该反应正向为△H>0;若该反应符合下图所示的关系,则在图中,Y轴是指CO2或H2的百分含量.
(2)能判断该反应达到化学平衡状态的依据是bc(多选扣分).
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2)正=v (H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9•c(CO2)•c(H2)═c(CO)•c(H2O),由此可以判断此时的温度为800℃.其它条件不变,升高温度,原化学平衡向正反应方向移动(填“正”或“逆”),容器内混合气体的密度不变(填“增大”、“减小”或“不变”),气体平均相对分子质量不变(填“增大”、“减小”或“不变”).
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡.若反应开始时CO与H2O的浓度分别为0.200mol/L和0.100mol/L,平衡时CO的转化率33.3%.
 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表:| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应正向为△H>0;若该反应符合下图所示的关系,则在图中,Y轴是指CO2或H2的百分含量.
(2)能判断该反应达到化学平衡状态的依据是bc(多选扣分).
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2)正=v (H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9•c(CO2)•c(H2)═c(CO)•c(H2O),由此可以判断此时的温度为800℃.其它条件不变,升高温度,原化学平衡向正反应方向移动(填“正”或“逆”),容器内混合气体的密度不变(填“增大”、“减小”或“不变”),气体平均相对分子质量不变(填“增大”、“减小”或“不变”).
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡.若反应开始时CO与H2O的浓度分别为0.200mol/L和0.100mol/L,平衡时CO的转化率33.3%.
17.下列各化合物的命名中正确的是( )
| A. | 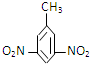 2,4-二硝基甲苯 2,4-二硝基甲苯 | B. | (CH3CH2)2CHCH33-甲基戊烷 | ||
| C. | 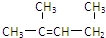 1,3-二甲基-2-丁烯 1,3-二甲基-2-丁烯 | D. | 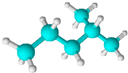 异戊烷 异戊烷 |
 亚硝酸(HN02)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多.回答下列问题:
亚硝酸(HN02)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多.回答下列问题: