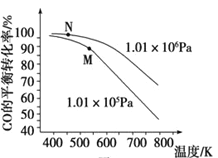
题目内容
【题目】X、Y、Z、W为原子序数递增的4种短周期元素,其中Y、Z为金属元素。X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如图所示反应关系(图中“一”相连的两种物质能发生反应)。下列判断正确的是
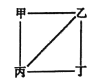
A. X是元素周期表中非金属性最强的元素
B. Z冶炼可通过电解其氯化物的方式获得
C. 4种原子中,Y离子半径最小
D. W的阴离子可能促进水的电离
【答案】D
【解析】Y、Z为金属元素,对应的最高价氧化物对应的水化物可发生反应,则应为氢氧化铝和氢氧化钠的反应,可知Y为Na、Z为Al,乙为NaOH,丙为Al(OH)3,X应为N,甲为HNO3,W可为为S、Cl,则丁可能为H2SO4、HClO4。由以上分析可知X为N、Y为Na、Z为Al、W为S或Cl,甲为HNO3,乙为NaOH,丙为Al(OH)3,丁为H2SO4或HClO4。A.X为N,元素周期表中非金属性最强的元素为F,故A错误;B.Z为Al,位于周期表第三周期ⅢA族,故B错误;C.4种原子中,半径最小的为N,Y为Na,原子半径最大,故C错误;D.如W为S,对应的离子为S2-,水解呈碱性,可促进水的电离,故D正确;故选D。

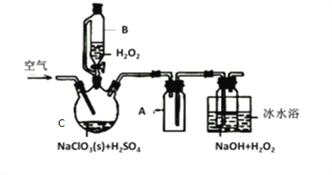
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去)

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | 33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)甲装置中仪器A的名称为___________。
(2)用甲装置制氯气,MnO4被还原为Mn2+,该反应的离子方程式为________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到__________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;②_______________________。
(4)乙装置的作用____________,如果缺少乙装置,可能发生的副反应的化学方程式为_________;己装置的作用是_____(填序号)。
A.防止空气中CO2气体进入戊装置
B.除去未反应的氯气,防止污染空气
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中不可用于检测是否产生SnCl2 的有_______(填序号)。
A.H2O2溶液 B.酸性高锰酸钾溶液 C.AgNO3溶液 D.溴水
(6)反应中用去锡粒1.19 g,反应后在戊装置的试管中收集到2.04 g SnCl4,则SnCl4的产率为_______(保留2位有效数字)。