题目内容
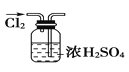
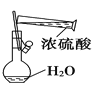
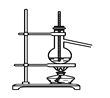
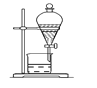
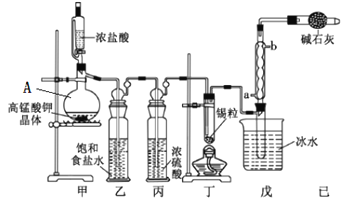
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去)
有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | 33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)甲装置中仪器A的名称为___________。
(2)用甲装置制氯气,MnO4被还原为Mn2+,该反应的离子方程式为________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到__________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;②_______________________。
(4)乙装置的作用____________,如果缺少乙装置,可能发生的副反应的化学方程式为_________;己装置的作用是_____(填序号)。
A.防止空气中CO2气体进入戊装置
B.除去未反应的氯气,防止污染空气
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中不可用于检测是否产生SnCl2 的有_______(填序号)。
A.H2O2溶液 B.酸性高锰酸钾溶液 C.AgNO3溶液 D.溴水
(6)反应中用去锡粒1.19 g,反应后在戊装置的试管中收集到2.04 g SnCl4,则SnCl4的产率为_______(保留2位有效数字)。
【答案】蒸馏烧瓶 10Cl-+16H++2MnO4-=5Cl2↑+8H2O+2Mn2+ 丁中充满黄绿色气体 促进四氯化锡挥发 除去氯气中混有的氯化氢气体 Sn+2HCl=SnCl2+H2 BC AC 78%
【解析】
SnCl4极易水解,应在无水环境下制备和保存。A装置制备氯气,由于浓盐酸易挥发,制备的Cl2中含有HCl及水蒸气,乙中盛放饱和食盐水除去HCl,丙中浓硫酸吸收水蒸气,干燥氯气,并用氯气排尽装置中空气,防止影响实验。氯气与Sn在丁处试管中反应生成SnCl4,反应生成SnCl4的为气态,在戊处冷却收集得到液态SnCl4,干燥管中碱石灰吸收未反应的氯气,防止污染环境,同时吸收空气中的水蒸气,防止进入收集SnCl4的试管使其水解。
(1)根据装置图可知:甲装置中仪器A的名称为蒸馏烧瓶,故答案为:蒸馏烧瓶;
(2)在A中KMnO4与浓盐酸发生氧化还原反应产生氯气,发生反应的离子方程式为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O,故答案为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O;
(3)若整个装置中充分氯气时,即丁装置充满黄绿色气体,再加热熔化锡粒合成SnCl4,加热丁装置,促进氯气与锡反应,同时使生成的SnCl4气化,有利于从混合物中分离出来,便于在戊处冷却收集,故答案为:丁中充满黄绿色气体;促进四氯化锡挥发;
(4) 乙装置的作用是除去氯气中混有的HCl杂质;
如果缺少乙装置,氯气中混有的HCl气体与Sn反应产生SnCl2与氢气,其方程式为Sn+2HCl=SnCl2+H2↑,使SnCl4产率降低,且氯气与氢气反应可能发生爆炸;
己装置是干燥管,干燥管中碱石灰吸收未反应的氯气,防止污染环境,同时吸收空气中的水蒸气,防止进入收集SnCl4的试管使其水解,故合理选项是BC;
(5)A. SnCl2易被氧化,H2O2溶液可以将Sn2+氧化,但没有明显现象,A项错误;
B. SnCl2易被氧化,与酸性高锰酸钾溶液混合,若褪色,则含有SnCl2,否则无SnCl2,B项正确;
C.使用AgNO3溶液可以检验氯离子,不能检验二价锡元素,C项错误;
D.与溴水混合,若橙色褪去,则说明含有SnCl2,SnCl2与溴水发生了氧化还原反应,否则无SnCl2,D项正确;故答案为:AC;
(5) 用去锡粒1.19g,其物质的量为n(Sn)=1.19g÷119g/mol=0.01mol,根据Sn原子守恒可知在理论生成SnCl4为0.01mol,则SnCl4的产率为![]() ×100%
×100%![]() 78%,故答案为:78%。
78%,故答案为:78%。

【题目】一定条件下,金属钠和CO2可制得金刚石:4Na+3CO2![]() 2Na2CO3+C(s,金刚石)
2Na2CO3+C(s,金刚石)
完成下列填空:
(1)上述反应中涉及的元素的原子半径从大到小的顺序为____。
(2)能证明碳元素与氧元素非金属强弱的事实是___(选填编号)。
a.最高价氧化物水化物的酸性 b.两种元素的气态氢化物的沸点
c.CO2中元素的化合价 d.气体氢化物受热分解的温度
(3)高压下,科学家成功地将CO2转化为具有类似SiO2结构的原子晶体,比较SiO2与CO2这两种原子晶体的熔沸点高低,并说明理由:___。
常压 | 熔点(℃) | 沸点(℃) |
钠 | 97.8 | 882.9 |
Na2CO3 | 851 | 1850分解 |
金刚石 | 3550 | … |
石墨 | 3850 | 4250 |
(4)若在2L密闭容器中,10min内金属钠减少了0.2mol,则CO2的平均反应速率为___。该反应在常压1000℃下进行,根据右表数据,该反应的平衡常数表达式K=___。
(5)若在2L密闭容器中,常压、1000℃下,起始时,下列物理量能说明该反应已达到平衡状态的是____。
a.气体的平均摩尔质量不变 b.3v消耗(Na)=4v生成(CO2)
c.气体的密度不变 d.![]() 的比值不变
的比值不变