题目内容
18.下列各项中表达正确的是( )| A. | F-的结构示意图: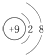 | B. | CH4分子的比例模型: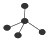 | ||
| C. | CCl4的电子式: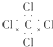 | D. | 乙烯的结构简式:CH2CH2 |
分析 A.氟离子质子数为9,核外电子数为10,根据离子结构示意图判断;
B.甲烷为正面体结构,由原子相对大小表示空间结构为比例模型;
C.四氯化碳中碳原子和氯原子均满足8电子稳定结构;
D.乙烯中含有碳碳双键,所以其结构简式中应体现其官能团.
解答 解:A.氟离子质子数为9,核外电子数为10,氟离子的结构示意图: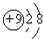 ,故A正确;
,故A正确;
B.甲烷为正面体结构,由原子相对大小表示空间结构为比例模型,则CH4分子正确的比例模型为: ,故B错误;
,故B错误;
C.四氯化碳中碳原子和氯原子均满足8电子稳定结构,正确的电子式为: ,故C错误;
,故C错误;
D.乙烯中含有碳碳双键,所以乙烯的结构简式为CH2=CH2,故D错误;
故选A.
点评 本题考查了化学用语的表示方法,题目难度中等,注意掌握比例模型、离子结构示意图、电子式、结构简式等化学用语的书写原则,试题侧重考查学生的规范答题能力.

练习册系列答案
相关题目
6.下列关于物质性质变化的比较,不正确的是( )
| A. | 酸性强弱:HIO4>HBrO4>HClO4 | B. | 原子半径大小:Na>Mg>Al | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 金属性强弱:Na>Mg>Al |
13.向平衡体系2NO+O2═2NO2中,通入18O组成的氧气,重新达到平衡后,18O存在于( )
| A. | 仅在O2中 | B. | 仅在NO2中 | C. | 仅在O2和NO2中 | D. | 平衡体系中 |
3.下列说法错误的是( )
| A. | 水玻璃可用于制备硅胶和木材防火剂 | |
| B. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| C. | 煤经过气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,PM2.5分散在空气中可能形成胶体或浊液 |
7.最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是( )
| A. | 该晶体类型是原子晶体 | |
| B. | 晶体的空间最小环共有6个原子构成 | |
| C. | 晶体中碳原子数与C-O化学键数之比为1:2 | |
| D. | 该晶体中碳原子和氧原子的个数比为1:2 |