题目内容
(12分)写出该反应的热化学方程式
(1)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量。
(2)0.2molC2H2(g)在氧气中完全燃烧生成CO2(g)和H2O(l),放出259.88kJ热量。
(3)1molC(石墨)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热 量。
量。
(4)0.3mol的气态高能原料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ的热量。
(1)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量。
(2)0.2molC2H2(g)在氧气中完全燃烧生成CO2(g)和H2O(l),放出259.88kJ热量。
(3)1molC(石墨)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热
 量。
量。(4)0.3mol的气态高能原料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ的热量。
(1)C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=-1366.8kJ.mol-1
(2)2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2598.8kJ.mol-1
(3)C(s)+H2O(g)=CO(g)+H2( g) △H=131.3kJ.mol-1
g) △H=131.3kJ.mol-1
(4)B2H6(g)+3O2(g)=B2O3(s)+3H2O(l) △H=-2165kJ.mol-1
(2)2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2598.8kJ.mol-1
(3)C(s)+H2O(g)=CO(g)+H2(
 g) △H=131.3kJ.mol-1
g) △H=131.3kJ.mol-1(4)B2H6(g)+3O2(g)=B2O3(s)+3H2O(l) △H=-2165kJ.mol-1
略

练习册系列答案
相关题目
 Si(s)+4HCl(g),该反应的反应
Si(s)+4HCl(g),该反应的反应 热△H为 ( )
热△H为 ( )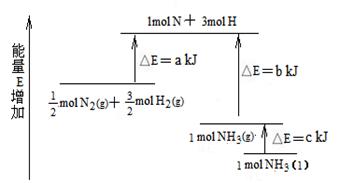
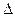 H=-570 kJ·mol-1;
H=-570 kJ·mol-1; 4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物
4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物 → SO2(g)+ Q1 kJ; S(g)+O2(g)
→ SO2(g)+ Q1 kJ; S(g)+O2(g) 2O (1),△H=-285.8 kJ·mol-1
2O (1),△H=-285.8 kJ·mol-1