题目内容
CH3—CH3→CH2=CH2+H2;有关化学键的键能如下。
试计算该反应的反应热
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ·mol—1) | 414.4 | 615.3 | 347.4 | 435.3 |
ΔH ==+125.6 kJ·mol—1。
ΔH =[6E(C-H)+E(C-C)]-[E(C=C)+4E(C-H)+E(H-H)]=(6×414.4+347.4) kJ·mol—1-(615.3+4×414.4+435.3) kJ·mol—1=+125.6 kJ·mol—1
这表明,上述反应是吸热的,吸收的热量为125.6 kJ·mol—1。
这表明,上述反应是吸热的,吸收的热量为125.6 kJ·mol—1。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
 量。
量。 12CO2(g)+4CO(g)+18H2O(l)
12CO2(g)+4CO(g)+18H2O(l)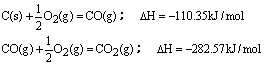

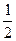 O2(g)=H2O(1) △H=-285.8kJ·mol-1
O2(g)=H2O(1) △H=-285.8kJ·mol-1