题目内容
6.如表对应关系不正确的是( )| 序号 | 俗称 | 主要成分 | 主要作用或用途 |
| A | 漂白粉 | Ca(ClO)2和CaCl2 | 可做漂白剂或环境消毒剂 |
| B | 硅胶 | H2SiO3 | 可做实验室或袋装食品、瓶装药品的干燥剂 |
| C | 石英 | SiO2 | 可做饰品、光纤材料以及半导体材料等 |
| D | 纯碱 | Na2CO3 | 可用于造纸、制玻璃等 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.漂白粉的主要成分是Ca(ClO)2和CaCl2,漂白粉可生成HClO,做漂白剂或环境消毒剂;
B.硅胶的主要成分是H2SiO3,硅胶具有吸湿性,常做干燥剂;
C.硅常用做半导体材料;
D.纯碱的主要成分是Na2CO3,是制造玻璃、造纸的常用材料.
解答 解:A.漂白粉的主要成分是Ca(ClO)2和CaCl2,漂白粉可生成HClO,做漂白剂或环境消毒剂,故A正确;
B.硅胶的主要成分是H2SiO3,硅胶具有吸湿性,常做干燥剂,故B正确;
C.硅常用做半导体材料,故C错误;
D.纯碱的主要成分是Na2CO3,是制造玻璃、造纸的常用材料,故D正确.
故选C.
点评 本题考查常见物质的主要成分及其重要用途,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
11.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=12的溶液:NO3-、I-、Na+、Al3+ | |
| B. | 0.1mol.L-1CH3COONa溶液:Mg2+、H+、Cl-、SO42- | |
| C. | Kw/c(H+)=0.1mol•L-1 的溶液:Na+、K+、SiO32-、NO3- | |
| D. | 0.1mol•L-1KMnO4溶液:Na+、Mg2+、N03-、S032- |
17.重水(D2O)是重要的核工业原料,下列说法错误的是( )
| A. | H2O与D2O互称同素异形体 | |
| B. | 1H218O与D216O的相对分子质量相同 | |
| C. | 氘(D)原子核外有1个电子 | |
| D. | 1H与D互为同位素 |
14.通常用来衡量一个国家石油化工发展水平标志的是( )
| A. | 甲烷的产量 | B. | 苯的产量 | C. | 乙醇的产量 | D. | 乙烯的产量 |
1.关于反应速率的说法中,正确的是( )
| A. | 反应速率用于衡量化学反应进行的快慢 | |
| B. | 决定反应速率的本质因素是反应温度 | |
| C. | 可逆反应达到化学平衡时,正逆反应速率都为0 | |
| D. | 增加反应物物质的量,能增大反应速率 |
11.下列说法正确的是( )
| A. | 蔗糖、麦芽糖水解都能得到2种物质 | |
| B. | 纤维素、淀粉和蛋白质都是高分子化合物 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 酯类和糖类均能发生水解反应 |
18.下列式子是某学生书写的C5H12的同分异构体的结构简式:①CH3CH2CH2CH2CH3 ②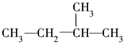 ③
③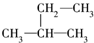 ④
④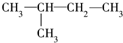 ⑤
⑤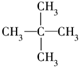
这些结构中出现重复的是( )
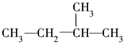 ③
③ ④
④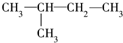 ⑤
⑤
这些结构中出现重复的是( )
| A. | ②和③ | B. | ④和⑤ | C. | ③和④ | D. | 均不重复 |
16.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 6.0 g甲醛分子中共用电子对数目为0.4NA | |
| B. | 标准状况下,22.4 L辛烷完全燃烧生成CO2分子数为8NA | |
| C. | 14g乙烯和环丙烷组成的混合气体中,含有的氢原子数目为2NA | |
| D. | 电解精炼铜时,若阴极得到电子0.2NA个,则阳极质量一定减少6.4g |
 .它的含氧官能团名称为羧基和醚基,能发生的有机反应类型有加成、取代反应.
.它的含氧官能团名称为羧基和醚基,能发生的有机反应类型有加成、取代反应.