题目内容
【题目】中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示. 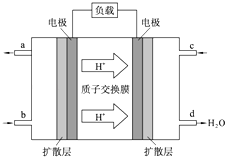
(1)该电池工作时,b口通入的物质为 , c口通入的物质为 .
(2)该电池负极的电极反应式为 .
(3)工作一段时间后,当6.4g甲醇完全反应生成CO2时,有NA个电子转移.
【答案】
(1)CH3OH;O2
(2)CH3OH+H2O﹣6e﹣=CO2+6H+
(3)1.2
【解析】解:(1.)根据装置可以知道d出生成大量的水,所以e口是通入的氧气,故b口通入的是CH3OH,所以答案是:CH3OH;O2;
(2.)乙醇发生氧化反应,在负极放电,总反应式为2CH3OH+3O2=2CO2+4H2O,正极电极反应为:3O2+12e﹣+12H+=6H2O,两式相减可得负极的电极反应式为2CH3OH﹣12e﹣+2H2O=2CO2+12H+ , 即CH3OH﹣6e﹣+H2O=CO2+6H+ . 所以答案是:CH3OH﹣6e﹣+H2O=CO2+6H+;
(3.)甲醇的物质的量为 ![]() =0.2mol,根据反应2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g),当消耗甲醇2mol时,转移电子为12mol,所以当6.4g甲醇完全反应生成CO2时,转移电子是
=0.2mol,根据反应2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g),当消耗甲醇2mol时,转移电子为12mol,所以当6.4g甲醇完全反应生成CO2时,转移电子是 ![]() ×12mol=1.2mol,转移电子数目是1.2NA , 所以答案是:1.2.
×12mol=1.2mol,转移电子数目是1.2NA , 所以答案是:1.2.

【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。

(1)上图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:____________________________________________________。
(2)已知化学键键能是形成或拆开1 mol化学键放出或吸收的能量,单位kJ/mol。若已知下列(右表)数据,试根据表中及图中数据计算N—H的键能____________kJ/mol。
化学键 | H—H | N≡N |
键能/kJ/mol | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ; ΔH1=-a kJ/mol ①
N2(g)+O2(g)===2NO(g) ; ΔH2=-b kJ/mol ②
若1 mol NH3还原NO至N2,则反应过程中的反应热ΔH3=________ kJ/mol(用含a、b的式子表示)。
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g) ===2Fe(s)+3CO2(g) ; ΔH1=-25 kJ/mol
②3Fe2O3(s)+CO(g)=== 2Fe3O4(s)+CO2(g) ; ΔH2=-47 kJ/mol
③Fe3O4(s)+CO(g) ===3FeO(s)+CO2(g) ;ΔH3=+640 kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式______________。
