题目内容
4.0.1mol/L的碳酸氢钠溶液存在下列离子,其中离子浓度最小的是( )| A. | Na+ | B. | H+ | C. | HCO3- | D. | OH- |
分析 碳酸氢钠为强碱弱酸盐,碳酸氢根离子部分水解,溶液显示碱性,则:c(Na+)>c(HCO3-)、c(OH-)>c(H+),溶液中各离子浓度大小为:c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),据此进行解答.
解答 解:碳酸氢钠溶液中,HCO3-的电离程度大于其水解程度,溶液显示碱性,则c(OH-)>c(H+),溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),所以选项中离子浓度最小的为c(H+),
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理及其影响为解答关键,注意掌握电荷守恒、物料守恒在判断离子浓度大小中的应用方法.

练习册系列答案
相关题目
14.在一定温度下的定容容器中,反应:A(s)+2B(g)?C(g)+D(g).下列不能表明反应达到平衡状态的是( )
| A. | 气体的压强不变 | B. | 气体平均相对分子质量不变 | ||
| C. | 气体的密度不变 | D. | B物质的量浓度不变 |
15.下列关于燃烧的说法正确的是( )
| A. | 燃烧一定要有氧气参加 | B. | 有发光现象的变化一定是燃烧 | ||
| C. | 燃烧一定有发光发热现象 | D. | 燃烧的生成物一定有气体 |
12.对于结构简式为如图的烃,下列说法正确的是( )
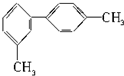

| A. | 分子中至少有6个碳原子处于同一平面上 | |
| B. | 分子中至少有8个碳原子处于同一平面上 | |
| C. | 分子中至少有10个碳原子处于同一平面上 | |
| D. | 分子中至少有14个碳原子处于同一平面上 |
19.以下各实验装置中,错误的是( )
| A. | 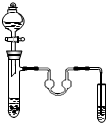 苯的溴代反应 | B. | 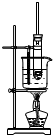 苯的硝化反应 | C. | 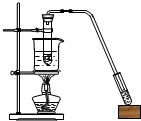 制取乙酸乙酯 制取乙酸乙酯 | D. |  制取乙烯 |
16.向100mL 18mol•L-1的H2SO4溶液中加入适量的铜片并加热,充分反应后,被还原的H2SO4的物质的量( )
| A. | 小于0.90 mol | B. | 等于0.90 mol | ||
| C. | 在0.90~1.80 mol之间 | D. | 大于0.90 mol |
13.下列有关实验及现象、原理的描述正确的是( )
| A. | 光照条件下,甲烷通入氯水中,发生了取代反应使黄绿色变浅 | |
| B. | 乙烯能使酸性高锰酸钾溶液褪色,也能使溴水褪色,两者反应原理一样 | |
| C. | 乙醛与新制氢氧化铜溶液混合好后,加热,得到砖红色沉淀 | |
| D. | 将一小粒钠投入盛有无水乙醇的小烧杯中,有气泡产生,比钠在水中的反应更剧烈 |
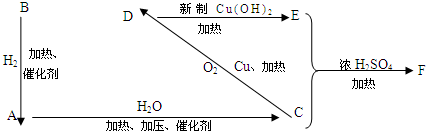
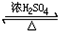 CH3COOCH2CH3+H2O,反应类型是取代反应.
CH3COOCH2CH3+H2O,反应类型是取代反应.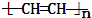 ,反应类型是加聚反应.
,反应类型是加聚反应.