题目内容
15.下列关于燃烧的说法正确的是( )| A. | 燃烧一定要有氧气参加 | B. | 有发光现象的变化一定是燃烧 | ||
| C. | 燃烧一定有发光发热现象 | D. | 燃烧的生成物一定有气体 |
分析 狭义燃烧的定义是:可燃物与氧气发生的剧烈的发光放热的氧化反应,广义燃烧的定义是可燃物跟助燃物(氧化剂)发生的剧烈的一种发光、发热的氧化反应,即燃烧是指任何发光发热的剧烈的反应,不一定要有氧气参加,据此解答即可.
解答 解:燃烧是可燃物跟助燃物(氧化剂)发生的剧烈的一种发光、发热的氧化反应,燃烧的广义定义:燃烧是指任何发光发热的剧烈的反应,不一定要有氧气参加,不一定生成气体,据此选项C正确,故选C.
点评 本题主要考查的是燃烧的定义,燃烧一定是发光放热的剧烈反应,不一定有氧气参加,比如氢气在氯气中也是燃烧,难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
6.在下列溶液中,各组离子一定能够大量共存的是( )
| A. | Cu2+、Mg2+、SO42- | B. | H+、Mg2+、CO32- | C. | Ag+、NO3-、Cl- | D. | Fe2+、H+、NO3- |
10.A、B、C、D是4种短周期元素,已知A、C同主族,B、C、D同周期,A的气态氢化物比C的气态氢化物稳定,B的阳离子比D的阳离子氧化性强,B的阳离子比C的阴离子少一个电子层.下列有关说法中,不正确的是( )
| A. | 原子序数 C>B>D>A | B. | 单质熔点 D>B,A>C | ||
| C. | 原子半径 D>B>C>A | D. | 简单离子半径 C>A>D>B |
7.“玉兔”号月球车用${\;}_{94}^{238}$Pu作为热源材料,下列关于${\;}_{94}^{238}$Pu的说法正确的是( )
| A. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U互为同位素 | |
| B. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu互为同素异形体 | |
| C. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U具有完全相同的化学性质 | |
| D. | ${\;}_{92}^{238}$Pu与${\;}_{92}^{239}$Pu具有相同的最外层电子 |
4.0.1mol/L的碳酸氢钠溶液存在下列离子,其中离子浓度最小的是( )
| A. | Na+ | B. | H+ | C. | HCO3- | D. | OH- |
5.有A、B、C三种金属,将A与B用导线联结起来,浸入电解质溶液中,B不易腐蚀.将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出.据此判断它们的活动性由强到弱的顺序是( )
| A. | B>A>C | B. | A>B>C | C. | A>C>B | D. | C>B>A |
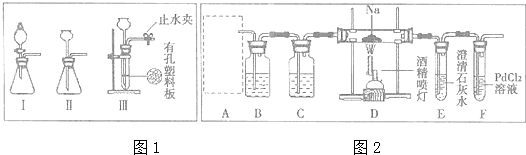
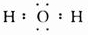
 .
.