题目内容
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:_______与盐酸反应最剧烈,______与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理_______说明理由:_____________________________。
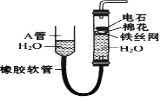
Ⅱ.利用下图装置可以验证非金属性的变化规律。
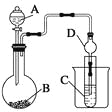
(3)仪器A的名称为____,干燥管D的作用是______________。
(4) 实验验证氯的非金属性大于硫:A中放浓盐酸、B中放KMnO4、C中盛放__________,离子方程式为____________。从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气.
(5)若要证明非金属性:C>Si,则A中加盐酸、B中加Na2CO3、C中加________,观察到C中溶液的现象为____________________。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________溶液的洗气瓶.
【答案】Ⅰ.(1)钾、铝
(2)不合理,因为一水合氨不是最高价氧化物对应的水化物
Ⅱ.(3)分液漏斗、防倒吸
(4) Na2S(其他答案合理也可);Cl2+ H2S ="S" + 2H++ 2Cl-(与上空答案相符);氢氧化钠溶液
(5)硅酸钠溶液,出现白色胶状物质,饱和碳酸氢钠溶液
【解析】试题分析:Ⅰ.(1)同一周期元素,元素的金属性随着原子序数增大而减弱,同一主族元素,元素金属性随着原子序数增大而增强,金属元素的金属性越强,其单质与水或酸反应越剧烈,金属性K>Na>Mg>Al,所以K与盐酸反应最剧烈,Al与盐酸反应最慢,故答案为:K;Al;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强,一水合氨不是N元素的最高价氧化物的水化物,所以不能比较金属性强弱,故答案为:不合理;因为一水合氨不是最高价氧化物对应的水化物;
Ⅱ.(3)A是分液漏斗,D为导致的干燥管,有缓冲作用,所以能防止倒吸,故答案为:分液漏斗;防倒吸;
(4)元素的非金属性越强,其单质的氧化性越强,同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,用浓盐酸和酸性高锰酸钾溶液制取氯气,氯气氧化硫化钠得到S,从而证明氯气氧化性大于S,则非金属性Cl>S,离子方程式为Cl2+H2S=S+2H++2Cl-;氯气有毒,不能直接排空,要进行尾气处理,氯气能和强碱NaOH溶液反应生成NaCl、NaClO而降低毒性;故答案为:Na2S溶液(其他答案合理也可);Cl2+H2S=S+2H++2Cl-;NaOH;
(5)元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,稀盐酸和碳酸钠反应生成二氧化碳,二氧化碳和硅酸钠溶液反应生成硅胶,产生白色胶状物质;因为盐酸具有挥发性,所以生成的二氧化碳中含有HCl,HCl也能和硅酸钠反应,应该除去,除杂时要除去杂质且不能引进新的杂质,用饱和的碳酸氢钠溶液除去HCl,故答案为:硅酸钠溶液;出现白色胶状物质;饱和碳酸氢钠溶液。

 名校课堂系列答案
名校课堂系列答案