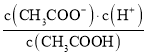题目内容
【题目】氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)![]() Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+H2O![]() HClO+H++Cl- K2=10-3.4
HClO+H++Cl- K2=10-3.4
HClO![]() H++ClO- Ka=?
H++ClO- Ka=?
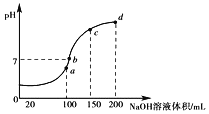
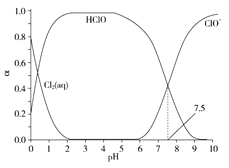
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是( )
A.Cl2(g)+H2O![]() 2H++ClO-+Cl- K=10-10.9
2H++ClO-+Cl- K=10-10.9
B.在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH-)
C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
【答案】C
【解析】
根据图象知,![]() ,当pH=7.5时
,当pH=7.5时![]() ,
,![]()
A. 将已知的三个式子相加可得A中方程式,所以![]() ,故A错误;
,故A错误;
B. 体系中存在电荷守恒![]() ,即
,即![]() ,根据方程式
,根据方程式![]() ,故
,故![]() ,故B错误;
,故B错误;
C.由图象可知,pH=6.5时![]() 比pH=7.5时要大,
比pH=7.5时要大,![]() 浓度越大,杀菌效果好,所以pH=6.5时杀菌效果比pH=7.5时好,故C正确;
浓度越大,杀菌效果好,所以pH=6.5时杀菌效果比pH=7.5时好,故C正确;
D. 夏季相比冬季温度高,![]() 易分解,所以杀菌效果不如冬季,故D错误;
易分解,所以杀菌效果不如冬季,故D错误;
答案选C。

练习册系列答案
相关题目