题目内容
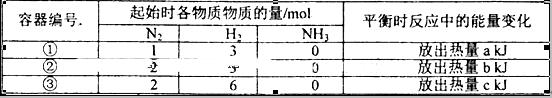
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)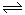 2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
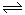 2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
| A.放出热量关系:a<b <92.4 |
| B.三个容器内反应的平衡常数:③>①>② |
| C.达平衡时氨气的体积分数:①>③ |
| D.N2的转化率:②>①>③ |
A
试题分析:A、①、②相比,②的氮气的浓度较大,氢气浓度相等,所以②的氢气的转化率高,放出的热量多,但氢气不会完全转化,所以放出的热量都小于92.4kJ,a<b <92.4正确;B、三个容器内反应的温度相同,对于同一反应,温度不变,化学平衡常数不变,错误;C、①、③相比,③的反应物浓度是①的2倍,所以③相当于在①平衡的基础上又正向移动,所以达平衡时氨气的体积分数:①<③,错误;D、由C分析,①、③相比,N2的转化率③>①;①、②相比,②的氮气的浓度较大,氢气浓度相等,根据增大一种反应物的浓度会增大另一种反应物的转化率,而自身转化率降低,所以N2的转化率:①>②,综合起来是③>①>②,错误,答案选A。

练习册系列答案
相关题目
 2C
2C x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求: CO(g)+H2(g);
CO(g)+H2(g); H2(g)+CO2(g)。
H2(g)+CO2(g)。 2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。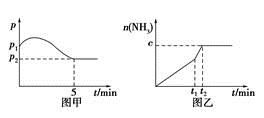
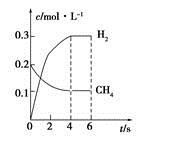
 CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如右图所示:0~4 s内,用CO(g)表示的反应速率为____________。
CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如右图所示:0~4 s内,用CO(g)表示的反应速率为____________。 2SO3(g),能增大正反应速率的措施是( )
2SO3(g),能增大正反应速率的措施是( ) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: 4NO(g)+6H2O(g),若化学反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[单位:mol/(L·s)]表示,则正确关系是( )
4NO(g)+6H2O(g),若化学反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[单位:mol/(L·s)]表示,则正确关系是( ) v(NH3)=v(O2)
v(NH3)=v(O2) v(O2)=v(H2O)
v(O2)=v(H2O)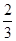 v(NH3)=v(H2O)
v(NH3)=v(H2O)