题目内容
19.相对分子质量为128的有机物A完全燃烧后只生成二氧化碳和水,若A含有一个六元碳环且能与NaHCO3溶液反应生成二氧化碳,则其环上的一溴代物有( )| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
分析 含有一个六元碳环且能与NaHCO3溶液反应生成二氧化碳,则A中含有-COOH,有机物A完全燃烧后只生成二氧化碳和水,说明没有碳氢氧以外的元素,A的相对分子质量为128的,A含有一个六碳环,6个碳原子式量为72,-COOH的式量为45,故分子含有1个-COOH,利用残余法可知,剩余基团或原子的总式量为128-72-45=11,故还原11个H原子,A的结构简式为 ,据此分析.
,据此分析.
解答 解:A含有一个六元碳环且能与NaHCO3溶液反应生成二氧化碳,则A中含有-COOH,有机物A完全燃烧后只生成二氧化碳和水,说明没有碳氢氧以外的元素,A的相对分子质量为128的,A含有一个六碳环,6个碳原子式量为72,-COOH的式量为45,故分子含有1个-COOH,利用残余法可知,剩余基团或原子的总式量为128-72-45=11,故还原11个H原子,A的结构简式为 ,环上的取代物,除了-COOH的邻、间、对位置外,羧基连接的碳也还有氢原子,可以取代,故其环上的一溴代物有4种,
,环上的取代物,除了-COOH的邻、间、对位置外,羧基连接的碳也还有氢原子,可以取代,故其环上的一溴代物有4种,
故选B.
点评 本题考查同分异构体、有机物的推断等,注意残余法确定有机物的结构是解题的关键.

练习册系列答案
相关题目
9.如图所示是一个有机物的核磁共振氢谱图,请你观察图谱,分析其可能是下列物质中的( )
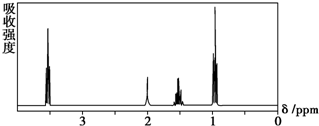

| A. | CH3CH2CH2CH3 | B. | (CH3)2CHCH3 | C. | CH3CH2CH2OH | D. | CH3CH2COOH |
10.据报道,碳纳米管是碳原子形成的大分子,其导电性是铜的1万倍;N5可以做烈性炸药.下列叙述正确的是( )
| A. | 金刚石和纳米管互为同分异构体 | B. | N5和N2互为同素异形体 | ||
| C. | 14C的质子数为14 | D. | C原子半径比N原子半径小 |
7.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的160%,则( )
| A. | a>b | B. | 物质A的转化率增大了 | ||
| C. | 物质A的质量分数减小了 | D. | 平衡向逆反应方向移动了 |
4.下列各组物质间,一定互为同系物的是( )
| A. | C2H6O和C4H10O | B. | C3H6O2和C4H8O2 | C. | C4H10和C10H22 | D. | C3H4和C4H6 |
8.下列各组离子,在所给条件下一定能大量共存的是( )
| A. | pH=0 的溶液中:Mg2+、Fe3+、NO3-、SO42- | |
| B. | 能和Ca2+生成沉淀的溶液中:Ba2+、K+、CH3COO-、Cl- | |
| C. | 能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、SO32- | |
| D. | 由水电离出的c(OH-)=1×10-13mol/L的溶液中:NH4+、Al3+、NO3-、Cl- |
9.判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示
(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出它们的结构式分别为 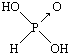 和
和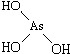 ,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:①H3PO3+2NaOH=Na2HPO3+2H2O; ②H3AsO3+3NaOH=Na3AsO3+3H2O.
| 名称 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
| 结构式 | Cl-OH |  | 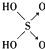 | 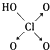 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 和
和 ,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:①H3PO3+2NaOH=Na2HPO3+2H2O; ②H3AsO3+3NaOH=Na3AsO3+3H2O.
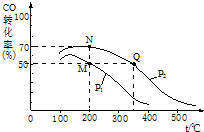 减少污染、保护环境是全世界最热门的课题.
减少污染、保护环境是全世界最热门的课题.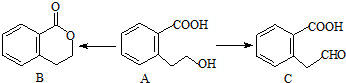
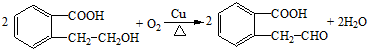 .
.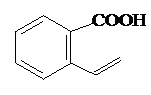 或
或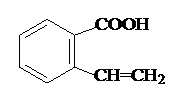 .
.