题目内容
18.下列各组物质中,既都含有共价键,却又都不属于共价化合物的一组是( )| A. | Na2O2 Na2O | B. | KClO NaOH | C. | Br2 HBr | D. | HF H2O |
分析 既都含有共价键,却又都不属于共价化合物说明应化合物中既含离子键又含共价键,由此分析解答.
解答 解:A、氧化钠中只存在离子键,不存在共价键,故A错误;
B、KClO和NaOH中既含有离子键又有共价键,是离子化合物,故B正确;
C、溴是单质,而溴化氢是共价化合物,故C错误;
D、HF和H2O都只含共价键的共价化合物,故D错误;
故选B.
点评 本题考查了化合物和化学键的关系,明确基本概念是解本题关键,根据化合物中存在的化学键来分析解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列反应中一定有白色沉淀生成的是( )
| A. | 将久置的亚硫酸钠溶液中加入氯化钡溶液再加入稀盐酸 | |
| B. | 向碳酸钠溶液中加入酸性氯化钙溶液 | |
| C. | 向亚硫酸钠溶液中通入氯气再加入氯化钡和稀盐酸 | |
| D. | 向亚硫酸钠溶液中加入稀硝酸后再加入氯化钡溶液 | |
| E. | 二氧化硫通入氯化钡溶液中 |
13.下列关于氧化还原反应中电子转移数目的判断不正确的是( )
| A. | 5.6g铁粉与氯气充分反应失去的电子数一定为0.3NA | |
| B. | 0.1mol Zn与含0.1mol HCl的盐酸充分反应,转移的电子数目为0.2NA | |
| C. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA | |
| D. | 向FeCl2溶液中通入Cl2,当有1molFe2+被氧化时,共转移的电子的数目为NA |
3.在25℃的条件下,将体积都为10mL,pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,测得稀释后溶液的pH均为5,则稀释时加入水的体积( )
| A. | a=b=10 mL | B. | a=b>10 mL | C. | a<b | D. | a>b |
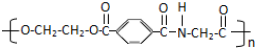 ,则这三种单体的结构简式为CH2OHCH2OH、
,则这三种单体的结构简式为CH2OHCH2OH、 、H2NCH2COOH.
、H2NCH2COOH.