题目内容
(15分)
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.用二氧化锰和浓盐酸制氯气的化学方程式是 。
Ⅲ.在收集氯气前,应依次通过盛有饱和食盐水和 的洗气瓶。
Ⅳ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,
充分反应后,将液体和剩余气体分离,进行如下研究。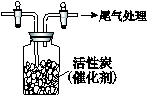
(1)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。
① 写出SO2Cl2与H2O反应的化学方程式 。
② 检验该溶液中Cl-的方法是 。
(2)继续研究反应进行的程度。用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。
① 该白色沉淀的成分是 。
② 写出SO2与Cl2反应的化学方程式,并阐述理由______。
(15分)
I.+6价(2分);
II.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O(2分);
MnCl2+Cl2↑+2H2O(2分);
Ⅲ.浓硫酸(2分);
Ⅳ.(1)① SO2Cl2+2H2O=H2SO4+2HCl (2分)。
② 取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加
HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-(2分);
(2)① BaSO4(2分);
② SO2+Cl2  SO2Cl2
SO2Cl2
由于白色沉淀是BaSO4,所以反应后的混合气体中必然存在SO2和Cl2两种气体。因此SO2和Cl2生成SO2Cl2的反应为可逆反应。(3分)
解析试题分析:I.SO2能被Cl2氧化生成SO2Cl2则氯元素的化合价是-1价,O一般表现为-2价,所以S的化合价是+6价;
II.实验室制取氯气的化学方程式为MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
Ⅲ.SO2Cl2极易水解,遇潮湿空气会产生白雾,所以氯气必须是干燥的,因此在收集氯气前,应依次通过盛有饱和食盐水和浓硫酸的洗气瓶。
Ⅳ.(1)①根据元素的化合价,判断SO2Cl2水解的产物是硫酸和氯化氢,化学方程式为 :SO2Cl2+2H2O=H2SO4+2HCl ;
②检验该溶液中Cl-的方法是:因为溶液中有硫酸存在,所以检验氯离子前应除去硫酸根离子,取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-;
(2)①若尾气中只含二氧化硫,被氢氧化钠吸收后滴加盐酸再滴加BaCl2溶液,不会产生白色沉淀。只含氯气也不会产生白色沉淀,所以尾气中有氯气和二氧化硫气体,白色沉淀是BaSO4
②SO2+Cl2  SO2Cl2,由上面的分析可知反应后的混合气体中必然存在SO2和Cl2两种气体,若该反应不是可逆反应,则不可能2种反应物同时有剩余,所以SO2和Cl2生成SO2Cl2的反应为可逆反应。
SO2Cl2,由上面的分析可知反应后的混合气体中必然存在SO2和Cl2两种气体,若该反应不是可逆反应,则不可能2种反应物同时有剩余,所以SO2和Cl2生成SO2Cl2的反应为可逆反应。
考点:考查氯气的实验室制法,化学方程式的判断与书写,试剂的选择,离子的检验,对实验现象的分析能力

 期末集结号系列答案
期末集结号系列答案在一只试管中装入NO2和NO混合气体a升(常温常压,下同。不考虑NO2转化为N2O4。),倒扣在水槽中,与水充分反应后剩余气体b升(不含水蒸气),再通入c 升O2,试管内刚好无气体剩余。
(1)b的值为 (用只含c的代数式表示)。
(2)填表。
| 表达要求 | 只含b的代数式 | 只含c的代数式 |
| a的取值范围 | | |
(3)写出只含c的代数式的推导过程。
(16分)亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛。以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示。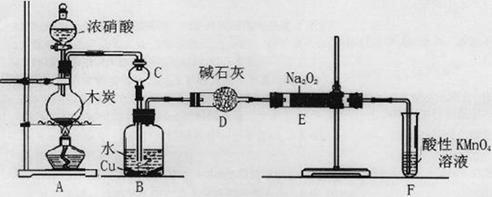
已知:室温下,① 2NO+Na2O2=2NaNO2;②酸性条件下,NO或NO2—都能与MnO4—反应生成NO3—和Mn2+,5NO2— + 2MnO4—+ 6H+=5NO3—+ 2Mn2++ 3H2O。
(1)A中观察到的现象__________________________。
(2)装置B中反应的离子方程式有____________________,_____________________。
(3)装置C的作用:____________________,装置F的作用:___________________。
(4)若无装置D,则E中产物除亚硝酸钠外还含有副产物________________________。(填化学式)
(5)NaNO2有像食盐一样的咸味,但能引起中毒。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O,根据上述反应,可以用试剂和生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐。进行实验时,必须选用的物质有__________________。
| A.自来水 | B.碘化钾淀粉试液 | C.淀粉 | D.白糖 E.食醋 F.白酒 |