题目内容
12.下列各组材料中,不能组成原电池的是( )| A | B | C | D | |
| 两极材料 | Zn片、石墨 | Zn片、Cu片 | Cu片、Ag片 | Fe片、Cu片 |
| 插入溶液 | H2SO4溶液 | 蔗糖溶液 | AgNO3溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据形成原电池的条件来分析,形成原电池的条件有:①两种活泼性不同的电极②电解质溶液③闭合回路④能自发进行氧化还原反应.
解答 解:A.因两电极材料不同,锌能与稀硫酸自发进行氧化还原反应,形成闭合回路,构成了原电池,故A不选;
B.蔗糖不导电,不能形成原电池,故B选;
C.铜为负极,银为正极,可形成原电池,故C不选;
D.铁为负极,铜为正极,可形成原电池,故D不选.
故选B.
点评 本题考查原电池知识,侧重于基础知识的考查,有利于培养学生的学习积极性和科学素养,难度不大,注意把握原电池的工作原理和组成条件.

练习册系列答案
相关题目
2.有一系列芳香族化合物,其中并四苯的一氯代物有( )
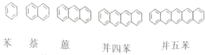

| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
3.仅用下表提供的仪器和用品能够实现相应目的是( )
| 选项 | 实验目的 | 仪器和用品 |
| A | 分离乙醇和乙酸乙酯的混合物 | 分液漏斗、烧杯、玻璃棒 |
| B | 检验溶液中是否含有SO42- | 试管、胶头滴管、Ba(NO3)2 |
| C | SO2既有氧化性,又有还原性 | 试管、胶头滴管、氯水、品红 |
| D | 配制100mLpH=2的盐酸 | 100mL容量瓶、烧杯、玻璃棒、胶头滴管、酸式滴定管、pH=1的盐酸 |
| A. | A | B. | B | C. | C | D. | D |
7.体积相同的甲乙两个容器中,分别充有等物质的量的SO2、O2,甲容器保持体积不变,乙容器保持压强不变,在相同温度下,发生2SO2(g)+O2(g)?2SO3(g)并达到平衡.则下列说法不正确的是( )
| A. | 平均反应速度:乙>甲 | B. | 平衡时SO3的物质的量甲>乙 | ||
| C. | 平衡时SO2的转化率:乙>甲 | D. | 平衡时混合气体的密度甲<乙 |
17.下列各组反应(表中物质均为反应物)起始时,产生H2的速率最大的是( )
| 编号 | 金属(粉末) | 物质的量(mol) | 酸的浓度 | 酸的体积 | 反应温度 |
| A | Mg | 0.1 | 6mol/L HNO3 | 10mL | 60℃ |
| B | Mg | 0.1 | 1.5mol/L HCl | 10mL | 60℃ |
| C | Fe | 0.1 | 3mol/L HCl | 10mL | 60℃ |
| D | Mg | 0.1 | 3mol/L HCl | 10mL | 60℃ |
| A. | A | B. | B | C. | C | D. | D |
1.水是制取氢气的常见原料,下列说法正确的是( )
| A. | H3O+的空间构型为三角锥形 | |
| B. | 冰中存在氢键,液态水中不存在氢键 | |
| C. | 冰晶体中,1mol水分子可形成4mol氢键 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
9.一种燃料电池,以镍板为电极插入KOH溶液,分别向两极通乙烷和氧气,电极反应为:C2H6+18OH--14e-=2CO32-+12H2O;7H2O+$\frac{7}{2}$O2+14e-=14OH-.有关推断不正确的是( )
| A. | 通氧气的电极为负极 | |
| B. | 参加反应的O2与C2H6的物质的量之比为7:2 | |
| C. | 电池工作一段时间后,KOH的物质的量浓度减小 | |
| D. | 电池工作时,溶液中OH-离子向正极移动 |

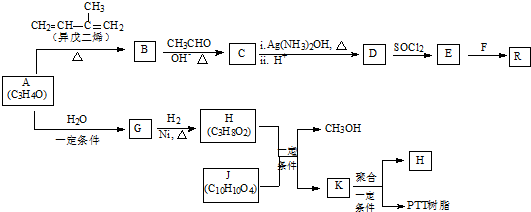
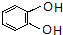 ,C的系统命名是3-溴丙烯(或3-溴-1-丙烯).
,C的系统命名是3-溴丙烯(或3-溴-1-丙烯).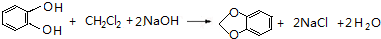 (或
(或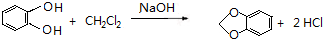 ).
).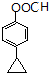 或
或 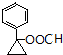 (任写一种).
(任写一种).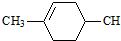 ═CHCOOCH2CH=CHCH2OOCH═
═CHCOOCH2CH=CHCH2OOCH═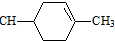
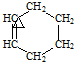
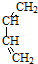 +
+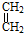 →
→
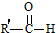 +
+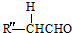 $→_{△}^{OH-}$R′CH
$→_{△}^{OH-}$R′CH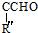 +H2O
+H2O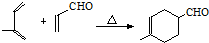 .
.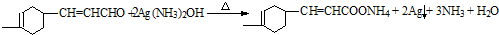 .
.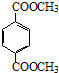 .
.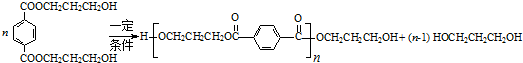 .
.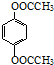 (邻、间、对三种中的任一种).
(邻、间、对三种中的任一种).