题目内容
18 g炭粉燃烧所得气体中CO占,CO2占;且C(s)+O2(g)===CO(g) ΔH=-110.35 kJ·mol-1, CO(g)+O2(g)===CO2(g) ΔH=-282.57 kJ·mol-1,与这些碳完全燃烧相比较,损失的热量是( )
| A.196.46 kJ | B.55.175 kJ |
| C.141.285 kJ | D.282.57 kJ |
C
18 g炭粉的物质的量为1.5 mol
题给两热化学方程式相加,得碳完全燃烧的热化学方程式:
C(s)+O2(g)===CO2(g) ΔH=-392.92 kJ·mol-1
生成气体中CO占,CO2占时,放热为: 110.35 kJ×0.5 mol +392.92 kJ×1mol="448.095" kJ;
若完全燃烧则生成CO2,放热为:392.92 kJ×1.5mol="589.38" kJ;
故损失了589.38 kJ-448.095 kJ="141.285" kJ
题给两热化学方程式相加,得碳完全燃烧的热化学方程式:
C(s)+O2(g)===CO2(g) ΔH=-392.92 kJ·mol-1
生成气体中CO占,CO2占时,放热为: 110.35 kJ×0.5 mol +392.92 kJ×1mol="448.095" kJ;
若完全燃烧则生成CO2,放热为:392.92 kJ×1.5mol="589.38" kJ;
故损失了589.38 kJ-448.095 kJ="141.285" kJ

练习册系列答案
相关题目
 。若加入少量醋酸钠固体,则CH3COOH
。若加入少量醋酸钠固体,则CH3COOH CH3COO-+H+向左移动,α减小,Ka变小
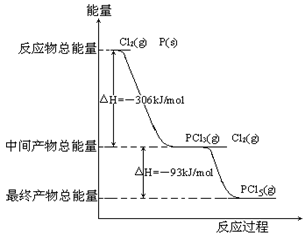
CH3COO-+H+向左移动,α减小,Ka变小 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
2Fe(s)+3CO(g),△H=+489.0 kJ/mol。 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表: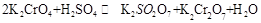
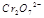 在水溶液中为红色,
在水溶液中为红色,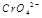 在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。
在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。 ;
;
 ,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用
,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用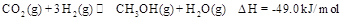
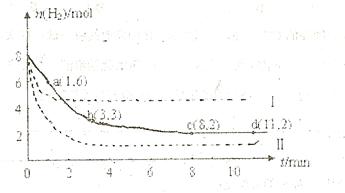
 充入一容积为2L的密闭容器中,测得H
充入一容积为2L的密闭容器中,测得H