题目内容
(6分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)在不同温度下,反应N2(g)+O2(g) 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
该反应的△H 0(填“>”、“=”或“<”)。
(2)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应:
N2(g)+O2(g) 2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
(3)科学家一直致力于研究常温常压下“人工固氮”的新方法。曾有实验报道:在常温、常压光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方程式如下:
2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热DH= 。 (用含a的代数式表示)
(1)在不同温度下,反应N2(g)+O2(g)
 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
(2)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应:
N2(g)+O2(g)
 2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)(3)科学家一直致力于研究常温常压下“人工固氮”的新方法。曾有实验报道:在常温、常压光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方程式如下:
2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热DH= 。 (用含a的代数式表示)
(1)> (2)2.5mol/L (3)(2a-1530)kJ·mol-
(1)根据表中数据可知,升高温度,平衡常数增大,所以反应是吸热反应,即△H>0.
(2) N2(g)+O2(g) 2NO(g)
2NO(g)
起始量(mol) 2.6 2.6 0
转化量(mol) x x 2x
平衡量(mol) 2.6-x 2.6-x 2x
根据该温度下的平衡常数可知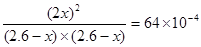
解得x=0.1mol,所以平衡时氮气的浓度为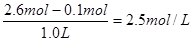
(3)考查盖斯定律的应用。将反应①N2(g)+O2(g) 2NO(g) DH=a kJ·mol-1和反应②2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1叠加,即①×2-②得到4NH3(g)+5O2(g)=4NO(g)+6H2O(1),所以其反应热是(2a-1530)kJ·mol-。
2NO(g) DH=a kJ·mol-1和反应②2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1叠加,即①×2-②得到4NH3(g)+5O2(g)=4NO(g)+6H2O(1),所以其反应热是(2a-1530)kJ·mol-。
(2) N2(g)+O2(g)
 2NO(g)
2NO(g)起始量(mol) 2.6 2.6 0
转化量(mol) x x 2x
平衡量(mol) 2.6-x 2.6-x 2x
根据该温度下的平衡常数可知
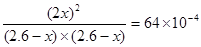
解得x=0.1mol,所以平衡时氮气的浓度为
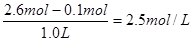
(3)考查盖斯定律的应用。将反应①N2(g)+O2(g)
 2NO(g) DH=a kJ·mol-1和反应②2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1叠加,即①×2-②得到4NH3(g)+5O2(g)=4NO(g)+6H2O(1),所以其反应热是(2a-1530)kJ·mol-。
2NO(g) DH=a kJ·mol-1和反应②2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1叠加,即①×2-②得到4NH3(g)+5O2(g)=4NO(g)+6H2O(1),所以其反应热是(2a-1530)kJ·mol-。
练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
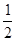 O2(g) = H2O(g) ΔH1=a kJ·mol-1?
O2(g) = H2O(g) ΔH1=a kJ·mol-1? 2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值: (写出 + 或-)。
2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值: (写出 + 或-)。 (g)+1/2O
(g)+1/2O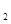 (g)=CO(g)+2H
(g)=CO(g)+2H H1=-35.6kJ·mol
H1=-35.6kJ·mol
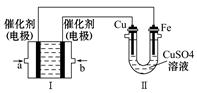
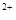 的物质的量浓度 。
的物质的量浓度 。