题目内容
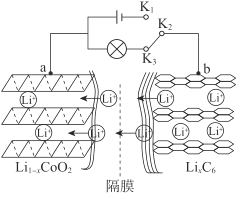
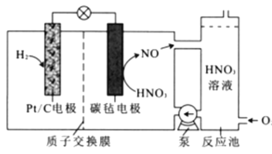
【题目】利用太阳能光伏电池电解水获得H2,工作示意图如图。下列分析不正确的是( )
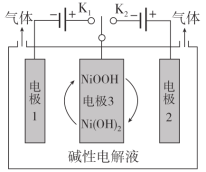
A.控制开关连接K1,电极1发生反应:2H2O+2e-=H2↑+2OH-
B.控制开关连接K2,电极3附近溶液的pH减小
C.通过控制开关连接K1或K2,可交替得到H2和O2
D.电极3的主要作用是通过NiOOH和Ni(OH)2相互转化实现电子转移
【答案】B
【解析】
当控制开关连接K1,电极1连接电源的负极,作阴极,溶液中的H2O得到电子,电极方程式为2H2O+2e-=H2↑+2OH-,电极3作阳极,发生氧化反应,Ni(OH)2转化为NiOOH,电极方程式为Ni(OH)2-e-+OH-=NiOOH+H2O。当控制开关连接K2,电极2连接电源的正极,作阳极,溶液中的OH-失电子,电极方程式为4OH--4e-=O2↑+2H2O;电极3作阴极,NiOOH转化为Ni(OH)2,电极方程式为NiOOH+e-+H2O=Ni(OH)2+OH-。
A.当控制开关连接K1,电极1连接电源的负极,作阴极,溶液中的H2O得到电子,电极方程式为2H2O+2e-=H2↑+2OH-,A正确,不选;
B.当控制开关连接K2,电极3作阴极,NiOOH转化为Ni(OH)2,电极方程式为NiOOH+e-+H2O=Ni(OH)2+OH-,电极附近产生OH-,pH增大,B错误,符合题意;
C.当控制开关连接K1时,电极1处H2O得到电子得到H2,当控制开关连接K2时,电极2处OH-失去电子得到O2,因此通过控制开关连接K1或K2,可交替得到H2和O2,C正确,不选
D.当控制开关连接K1,Ni(OH)2转化为NiOOH;当控制开关连接K2,NiOOH转化为Ni(OH)2。电极3处NiOOH和Ni(OH)2相互转化实现了电子转移,D正确,不选;
答案选B。

【题目】CO2的富集与转化是当今环境研究的热点。
(1)化石燃料的燃烧是使大气CO2浓度增加的原因之一。汽油中含有辛烷(C8H18),1molC8H18(l)完全燃烧生成CO2(g)和H2O(l),放出5518kJ热量。写出C8H18完全燃烧的热化学方程式:__。
(2)一种富集CO2的过程如图所示。
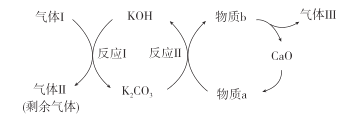
①气体Ⅰ、Ⅱ、Ⅲ中,CO2浓度最高的是___。
②反应Ⅱ的化学方程式是__。
(3)一定条件下,CO2和H2反应能生成C2H4,实现CO2向能源物质的转化。
已知:2CO2(g)+6H2(g)C2H4(g)+4H2O(g) ΔH<0
①上述反应的ΔH可根据C2H4(g)+3O2(g)=2CO2(g)+2H2O(g)和__反应的焓变计算。
②研究温度和压强对CO2的平衡转化率的影响,结果如图所示。
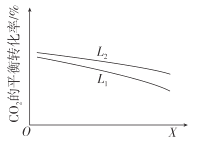
X代表的物理量是__。比较L1与L2的大小,并说明依据__。
③相同条件下,CO2和H2还能发生其它反应:
反应a:CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
反应b:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
……
Fe和Co(钴)可作为该反应的催化剂。改变铁钴的物质的量比,测定相同时间内CO2的消耗率和含碳产物的占比,结果如下:
n(Fe):n(Co) | CO2消耗率/% | 含碳产物占比/% | ||
CO | C2H4 | CH4 | ||
100:0 | 1.1 | 100 | 0 | 0 |
50:50 | 30.5 | 36.8 | 20.3 | 42.9 |
0:100 | 69.2 | 2.7 | 0.2 | 97.1 |
结合数据,推测催化剂中钴的作用:__。