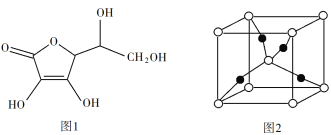
题目内容
【题目】下列有机物分子中,不可能所有原子在同一平面内的是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】B
【解析】
A.![]() 分子中平面分子,分子在所有原子在同一平面上,A不符合题意;
分子中平面分子,分子在所有原子在同一平面上,A不符合题意;
B.甲苯可看作是苯分子中的一个H原子被甲基取代产生的物质,也可以看成是甲烷分子中的1个H原子被苯基取代产生的物质。苯分子是平面分子,由于甲烷是正四面体结构的分子,若某一平面通过C原子,分子中最多有2个顶点在同一平面,因此甲苯分子中不可能所有原子都在同一平面上,B符合题意;
C.苯乙烯可看作是苯分子中的H原子被乙烯基-CH=CH2取代产生的物质,由于苯分子、乙烯分子都是平面分子,两个平面共直线,可能所有原子在同一平面上,C不符合题意;
D.苯乙炔可看作中苯分子中的1个H原子被乙炔基-C≡CH取代产生的物质,乙炔中与苯环连接的C原子取代苯分子中H原子的位置,在苯分子的平面内,由于苯分子是平面分子,乙炔是直线型分子,一条直线上2点在某一平面上,则直线上所有点都在这个平面上,因此所有原子在同一平面内,D不符合题意;
故合理选项是B。

【题目】2019年12月中旬以来,新型冠状病毒肺炎(NCP)肆虐全球,酒精、84消毒液、双氧水、过氧乙酸等化学品是常用的消毒剂,能够杀死新型冠状病毒。
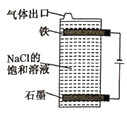
Ⅰ.如图是简易84消毒液发生器,写出该电解池中发生的总反应的化学方程式:__。
Ⅱ.过氧化尿素是一种新型漂白剂、消毒剂,漂白、消毒的效果优于H2O2和过氧乙酸。
某工业用过氧化尿素的部分参数见下表:
分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 500g·L-1 |
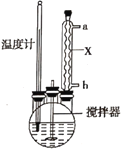
合成过氧化尿素的流程及反应器的示意图如图:

回答下列问题:
(1)流程中操作①的名称为__,仪器X的名称是__。
(2)流程中操作②的具体过程是__。
A.盐析、过滤 B.减压蒸馏、结晶、过滤 C.分液、过滤 D.常压蒸馏、萃取
(3)搅拌器选用的材质是玻璃而不是铁质的原因是__。
(4)为测定产品中活性氧的含量(含双氧水34%,则其中活性氧为16%),一般采用KMnO4标准溶液进行滴定,但由于KMnO4的强氧化性,其溶液很容易被空气或水中的少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液有如下步骤:
a.利用氧化还原滴定方法,在70~80℃条件下用基准试剂纯度高、相对分子质量较大、稳定性较好的物质)溶液标定其浓度。
b.过滤得到的KMnO4溶液贮存于棕色试剂瓶中并放在暗处。
c.称取稍多于所需量的KMnO4固体溶于水中,将溶液加热并保持微沸![]() 。
。
d.用微孔玻璃漏斗过滤除去难溶的MnO(OH)2。
①请按照正确的流程对上述步骤进行排序__(填字母)。
②在下列物质中,用于标定KMnO4溶液的基准试剂最好选用__。
A.H2C2O4·2H2O B.FeSO4 C.浓盐酸 D.Na2SO3
③若准确称取Wg你选的基准试剂溶于水配成500mL溶液,取25.00mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。称取干燥样品1.2g,溶解后置于锥形瓶中加入1mL6mol·L-1的硫酸,然后用上述KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如下:
实验序号 | 1 | 2 | 3 | |
KMnO4溶液体积 (mL) | 滴定前读数 | 0.00 | 0.00 | 1.00 |
滴定后读数 | 19.90 | 22.70 | 21.10 |
产品中活性氧的质量分数为__(用含字母的最简等式表示)。
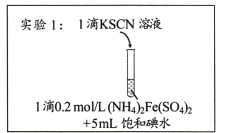
【题目】某研究小组查阅资料发现Fe3+与I-的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在Fe3+,并据此设计实验1(如下图所示),发现溶液未变红。该小组对溶液未变红的原因进行了如下探究。
I.初步探究
实验2:用煮沸冷却后的蒸馏水重新配制两种饱和溶液进行实验,实验记录如下表。
编号 | 饱 和 (NH4)2Fe(SO4)2溶液 | 饱和碘水 | 石蜡油 | 操作 | KSCN溶液 | 现象 |
2-1 | 1滴 | 5mL | 1mL | 不加热 | 1滴 | 无明显现象 |
2-2 | 1滴 | 5mL | 1mL | 加热一段时间后冷却 | 1滴 | 无明显现象 |
(1)研究小组同学根据所查阅资料写出的Fe3+与I-反应的离子方程式为____。
(2)实验2中,加入石蜡油的目的是____。
(3)小组同学做出推断:反应速率不是导致实验1中溶液未变红的主要原因,他们的理由是___。
II.查阅资料,继续探究
(资料)AgSCN为不溶于水的白色固体。
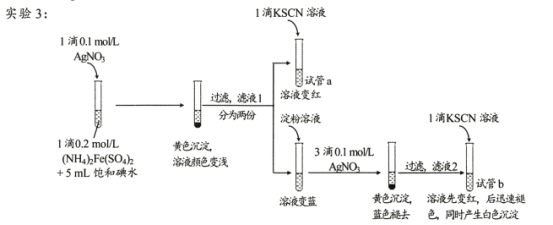
(4)试管a的实验现象说明滤液l中含有____。
(5)试管b中,加入KSCN溶液后所产生实验现象的原因是 ___。
(6)甲同学对实验3提出了质疑,认为其实验现象并不能证明I2氧化了Fe2+。他提出如下假设:i.可能是AgNO3氧化了Fe2+;ii.可能是空气中的O2氧化了Fe2+。 他设计、实施了实验4,实验记录如下表。
编号 | 实验操作 | 实验现象 |
4 | 在试管中加入1滴0.2mol/L(NH4)2Fe(SO4)2溶液,5mL蒸馏水,1滴试剂a,一段时间后加入1滴KSCN溶液 | 溶液不变红 |
①试剂a是 ___。
②依据实验4,甲同学做出判断:______________________
(7)根据实验1~4所得结论是____。