题目内容
【题目】下列各表述正确的是( )
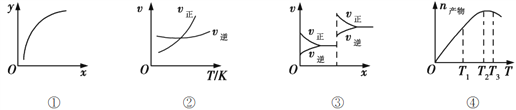
A. 图①表示在恒容容器中MgSO4(s) + CO(g)![]() MgO(s) + CO2(g) + SO2(g),横坐标代表硫酸镁的质量,纵坐标可代表CO的转化率
MgO(s) + CO2(g) + SO2(g),横坐标代表硫酸镁的质量,纵坐标可代表CO的转化率
B. 图②表示其他条件一定时,反应A(g)+3B(g)![]() 2C(g)的反应速率随温度变化的图像,正反应ΔH>0
2C(g)的反应速率随温度变化的图像,正反应ΔH>0
C. 图③对应的反应一定是非等体积反应加压后平衡移动的变化情况
D. 恒压密闭容器中加入一定量A、B,发生反应A(g)+3B(g)![]() 2C(g),图④表示反应过程中不断升高温度,产物C物质的量变化规律,则正反应方向吸热
2C(g),图④表示反应过程中不断升高温度,产物C物质的量变化规律,则正反应方向吸热
【答案】B
【解析】A、硫酸镁是固体,固体物质的量的增减对化学平衡没有影响,所以CO的转化率不变,因此A错误;B、分析图象可知,随温度的升高,ν正>ν逆,即平衡向右移动,则正反应吸热,即ΔH>0,所以B正确;C、由于气体物质受压强影响较大,所以图象表示的是有气体物质参与的反应前后气体体积不相等的反应加压后平衡移动的情况,故C错误;D、随温度的升高,反应速率加快,当产物C的物质的量最大时达到平衡状态,但继续升温,产物C的量却在减小,说明升高温度,平衡向左移动,则其正反应为放热反应,所以D错误。本题正确答案为B。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目