题目内容
4.某有机物A的结构为Br-CH2-CH=CH-CH2OH,它不可能发生的反应是( )| A. | 与硝酸银溶液反应生成AgBr | B. | 使溴的四氯化碳溶液褪色 | ||
| C. | 与金属钠反应放出氢气 | D. | 使高锰酸钾溶液褪色 |
分析 该物质中含有碳碳双键、醇羟基、溴原子,具有烯烃、醇和卤代烃性质,能发生加成反应、加聚反应、取代反应、氧化反应、水解反应等,据此分析解答.
解答 解:A.该物质中不含自由移动的溴离子,所以不能与硝酸银溶液反应,故A错误;
B.含有碳碳双键,所以能和溴发生加成反应而使溴的四氯化碳溶液褪色,故B正确;
C.含有醇羟基,能和钠反应生成氢气,故C正确;
D.含有碳碳双键,所以能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故D正确;
故选A.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系即可解答,侧重考查醇、烯烃、卤代烃性质,注意不能发生消去反应,为易错点.

练习册系列答案
相关题目
17.下列有关糖类、油脂、蛋白质的叙述正确的是( )
| A. | 淀粉和纤维素的相对分子质量相同,互称同分异构体 | |
| B. | 糖类、油脂、蛋白质都属于天然高分子化合物 | |
| C. | 油脂在酸性条件下和碱性条件下都可以水解,且水解产物均相同 | |
| D. | 在允许加热的条件下,可以用氢氧化铜鉴别葡萄糖、乙酸、乙醇 |
15.在CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O的平衡体系中,加入一定量的C2H518OH,当重新达到平衡时,18O原子应存在于( )
| A. | 乙酸乙酯中 | B. | 乙酸中 | ||
| C. | 水中 | D. | 乙酸、乙酸乙酯和水中 |
12.下列物质的分离方法不正确的是( )
| A. | 用结晶的方法分离汽油和水 | |
| B. | 用过滤的方法除去氯化钠溶液中的泥沙 | |
| C. | 用重结晶的方法从含有少量氯化钠的硝酸钾溶液中提取硝酸钾 | |
| D. | 蒸馏法分离乙酸(沸点118.)和乙酸乙酯(沸点77.1.) |
19.将乙醛和乙酸分离的正确方法是( )
| A. | 加热蒸馏 | |
| B. | 先加入烧碱溶液,之后蒸馏出乙醛;再加入浓硫酸,蒸馏出乙酸 | |
| C. | 加入Na2CO3后,通过萃取的方法分离 | |
| D. | 利用银镜反应进行分离 |
9.在一定的温度下,可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A. | C分解速率与B生成速率相等 | |
| B. | A、B、C的浓度不再变化 | |
| C. | 单位时间生成nmol A,同时生成3nmol B | |
| D. | A、B、C的分子数之比为1:3:2 |
16.关于如图所示的原电池,下列说法正确的是( )
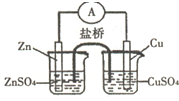

| A. | 电子从锌电极通过电流表流向铜电极 | |
| B. | 盐桥中的阴离子向硫酸铜溶液中迁移 | |
| C. | 取出盐桥后,电流计的指针仍发生偏转 | |
| D. | 铜电极上发生的电极反应是2H++2e-═H2↑ |
13.在给定条件下,下列加线的物质在化学反应中几乎能被完全消耗的是( )
| A. | 8.7 g二氧化锰与50 mL8 mol•L-1浓盐酸共热制取氯气 | |
| B. | 19.2 g铜与100 mL12 mol•L-1的硝酸反应 | |
| C. | 常温下,将5.4 g铝片投入20 mL18 mol•L-1的硫酸中 | |
| D. | 将足量的Cu置于50 mL18 mol•L-1H2SO4溶液中加热 |
14.碳酸钠溶液中存在着Na2CO3+H2O?NaHCO3+NaOH的平衡,加热蒸干溶液,得到的固体是( )
| A. | Na2CO3 | B. | NaHCO3和NaOH | C. | NaOH | D. | Na2CO3和NaOH |