��Ŀ����
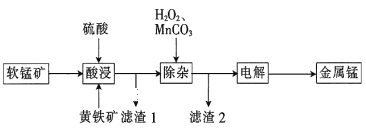
����Ŀ��һ�������̿�(��Ҫ�ɷ�ΪMnO2��SiO2��Al2O3)�ͻ�����(FeS2��SiO2)Ϊԭ��ұ�������̵Ĺ���������ͼ��ʾ��
��֪��ؽ�������[c(Mn+)=0.1molL-1]�γ��������������pH���£�
�������� | Fe3+ | Mn2+ | Al3+ |
��ʼ������pH | 2.7 | 8.3 | 3.2 |
������ȫ��pH | 3.7 | 9.8 | 5.0 |
�ش��������⣺
��1��MnO2���������������ᣬ������Fe2+��������ȴ���ܽ⣬д���÷�Ӧ�����ӷ���ʽ��___��
��2������1�ijɷֳ���SiO2�⣬����һ�ֵ���ɫ��������___(�ѧʽ)��
��3�����Ӳ����м����MnCO3��������___���ù����������ҺpH�ķ�Χ��___������pH���ù��ߣ����˻�ʹ�̵IJ��ʻή�ͣ���������___��
��4���ö��Ե缫���е�⣬���տ�ʼʱ�����ĵ缫��ӦʽΪ___�����������ĵ������Һ�ɷ���___(��������������������������)�������ʹ�á�
���𰸡�MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O S ������Һ��pH��ʹFe3+��Al3+��ȫ���� 5.0��pH��8.3 ��ʹAlԪ���γ�AlO2-������Һ�ж���������� Mn2++2e-=Mn ���
��������
�������У��������ܽ����̿�ͻ�����Al2O3��FeS2�ܽ����Al3+��Fe2+��MnO2��SiO2���ܽ⣬�����⣨1����2����֪��MnO2��Fe2+��S22-�������з���������ԭ��Ӧ����Mn2+��Fe3+��S��ʹMnO2Ҳ�ܽ�����Һ�У���������I����Ҫ�ɷ���SiO2��S��������Һ�к���Al3+��Mn2+��Fe2+��Fe3+��Ȼ������Һ�м���H2O2��Ŀ����Ϊ�˽�Fe2+ȫ��ת��ΪFe3+���ټ���MnCO3���Ե�����ҺpH��5.0��pH��8.3��ʹ��Fe3+��Al3+��ȫ�����������Ϳ��Ի�ô�����MnSO4��Һ����������2����Ҫ�ɷ���Fe(OH)3��Al(OH)3���ٵ�����õ�MnSO4��Һ���ɵõ�����Mn��
��1��MnO2����ǿ�����ԣ�Fe2+���л�ԭ�ԣ������������з���������ԭ��Ӧ:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��
��2��FeS2��S��-1�ۣ�Ҳ���н�ǿ�Ļ�ԭ�ԣ����Ա�MnO2����ΪS���������Ѿ���֪����1����SiO2֮�⣬�����е���ɫ���ʣ���ֻ��S�������⣻
��3�����Ӳ����м����MnCO3��������ʹFe3+��Al3+��ȫ���������ݱ����ṩ����Ϣ��֪����Ҫ����ҺpH���Ƶķ�ΧΪ5.0��pH��8.3������ҺpH���ߣ�Al(OH)3���γ�AlO2-���ܽ��Һ�У�ʹ�����õ�MnSO4��Һ�������ʣ������룻
��4�����ʱ���������ҺΪMnSO4��Һ��������ӦΪ��Mn2++2e-=Mn��������ӦΪ��2H2O-4e-=4H++O2�����ɴ˿��Կ������������Mn֮�⣬����H2SO4���ʵ��������ĵ������Һ�ɷ�������������ʹ�á�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ�������£�ijͬѧ�������백ˮ�������ϣ����ǰ������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±����ݱ�����������˵����ȷ���ǣ� ��
ʵ���� | ��ˮŨ��/mol��L��1 | ����Ũ��/mol��L��1 | �����ҺpH |
�� | 0.1 | 0.1 | pH��5 |
�� | c | 0.2 | pH��7 |
�� | 0.2 | 0.1 | pH��7 |
A.����c��0.2
B.�١���������Һ�е�![]() ����>��
����>��
C.����������Һ��c(NH4+)+c(H+)��c(OH��)+c(NH3��H2O��
D.�������û����Һ����ˮ�������c(H��)��1��10��9 mol��L��1